Хронические расстройства питания (дистрофии) – заболевания детей раннего возраста, характеризующиеся нарушениями усвоения питательных веществ тканями организма, что сопровождается нарушением гармоничного развития ребенка.
Содержание
- 1 Классификация хронических расстройств питания у детей
- 2 Гипотрофия
- 3 Гипостатура
- 4 Причины. Клинические проявления
- 5 Лечение
- 6 Паратрофия
- 7 Причины. Симптомы заболевания
- 8 Диагностика паратрофии
- 9 Лечение. Принципы диетотерапии
- 10 Профилактика паратрофии
- 11 Сестринский процесс при хронических расстройствах пищеварения
Классификация хронических расстройств питания у детей
Тип дистрофии:
-гипотрофия (отставание массы тела от роста);
-паратрофия (преобладание массы тела над ростом или равномерно избыточная масса тела и рост);
-гипостатура (равномерное отставание массы и роста).
Степень тяжести: первая, вторая и третья.
Гипотрофия
Гипотрофия – это хроническое расстройство питания и пищеварения, сопровождающееся нарушением обменных и трофических функций организма и характеризующееся снижением толерантности к пище и иммунобиологической реактивности, задержкой физического и психомоторного развития.
Врожденная (внутриутробная) гипотрофия – это хроническое расстройство питания плода, которое сопровождается отставанием физического развития, метаболическими нарушениями, понижением иммунологической реактивности, вследствие недостаточности плацентарного кровообращения, воздействие неблагоприятных факторов со стороны матери. Клинически проявляется истончением подкожной жировой клетчатки, увеличением кожных складок на шее, конечностях, вокруг суставов и уменьшением их толщины, общей гипотонией, периоральным цианозом, одышкой, наличием четко отграниченных костных образований, снижением массо-ростового индекса (ниже 60).
Приобретенная гипотрофия – это хроническое расстройство питания, характеризующееся прекращением или замедлением нарастания массы тела, прогрессирующим исчезновением подкожно-жирового слоя, нарушением пропорций тела, функции пищеварения, обмена веществ, снижением специфических и неспецифических факторов защиты организма, предрасположенностью к развитию других заболеваний и задержкой нервно-психического развития. Причины: недостаточное питание(недоедание, затруднение при питании), инфекционные факторы, токсические факторы, анорексия как следствие психических расстройст, нарушения переваривания, повышенные потребности в питании,заболевания обмена веществ, ИДС.
В патогенезе ведущая роль принадлежит глубоким нарушениям всех видов обмена веществ и изменениям со стороны внутренних органов. Под влиянием предрасполагающих факторов отмечается подавление секреции пищеварительных соков. Пищеварительные вещества, поступающие в организм, перестают перевариваться и усваиваются не полностью. Снижается порог переносимости (толерантности) пищи, легко возникают нарушения моторики желудочно-кишечного тракта, пища задерживается в желудке, появляются упорные поносы, сменяющиеся «голодными» поносами. В результате, в организм поступает недостаточное количество полноценного белка, витаминов, микроэлементов, что нарушает синтез ферментов, гормонов, гуморальную и эндокринную регуляцию процессов обмена. Диспротеинемия, дефицит ферментов и витаминов, особенно аскорбиновой кислоты, снижает активность тканевого обмена, потребления кислорода тканями и приводит к накоплению недоокисленных продуктов обмена с развитием метаболического ацидоза, активизируется перекисное окисление липидов, в крови накапливаются свободнорадикальные соединения, повреждающие клеточные мембраны и нарушающие процессы обмена на клеточном уровне. Понижается сопротивляемость организма и развивается состояние эндогенного токсикоза. На этом фоне легко присоединяется вторичная инфекция и может развиться токсико-септическое состояние, являющееся наиболее частой причиной летального исхода.
Классификация основана на оценке дефицита массы тела:
I-я степень – дефицит составляет 11-20%, II-я – 21-30%, III-я – 31% и более.
Клинические проявления:
синдром трофических нарушений (дефицит массы тела, в меньшей степени – длины тела, нарушение пропорциональности телосложения, нарушение эластичности кожи, тургора тканей, признаки гиповитаминоза, истончение подкожно-жирового слоя и мышц),
понижение пищевой толерантности(снижение аппетита вплоть до анерексии)
снижение иммунобиологической реактивности(анемия, ИДС) и симптомы изменения функционального состояния ЦНС (нарушение эмоционального тонуса и нервно-рефлекторной возбудимости, мышечная гипо- и дистония, гипорефлексия, темповое отставание психомоторного развития).
Клиническая симптоматика зависит от степени дефицита массы тела.
Гипотрофия I степени выявляется, как правило, только при внимательном осмотре ребенка. Обычно состояние его удовлетворительное, аппетит умеренно снижен, кожа гладкая, эластичная, бледная, внутренние органы и физиологические отправления без видимых отклонений. Снижен тургор тканей и толщина подкожно-жировой клетчатки на животе, но на лице и конечностях сохранена. При дополнительном обследовании, отмечаются диспротеинемия и снижение активности пищеварительных ферментов.
Гипотрофия II степени характеризуется снижением активности и эмоционального тонуса ребенка, апатией, вялостью, адинамией, задержкой психомоторного и речевого развития, выраженным снижением аппетита. Кожные покровы бледные, сухие, шелушатся, снижены эластичность кожи и тургор тканей, выражена мышечная гипотония. Подкожно-жировая клетчатка отчетливо уменьшена или отсутствует на животе и конечностях, сохранена на лице. Кривая нарастания массы тела уплощена. Часто отмечаются тахипноэ, аритмия дыхательных движений, приглушенность сердечных тонов, склонность к тахикардии и гипотонии, нарушения терморегуляции. При насильственном кормлении возникает рвота, нередко наблюдаются запоры. Указанные симптомы сопровождаются гипохромной анемией, гипо- и диспротеинемией, значительным снижением активности пищеварительных ферментов. Часто присоединяются интеркуррентные заболевания, осложняющиеся отитом, пиелонефритом, пневмонией.
Гипотрофия III степени сопровождается значительными нарушениями общего состояния ребенка: отмечаются сонливость, безучастность к окружающему, раздражительность, негативизм, повышенная плаксивость, резкое отставание в психомоторном развитии, утрата уже приобретенных навыков и умений, полная анорексия. По внешнему виду ребенок похож на скелетик, обтянутый сухой кожей бледно-серого цвета, свисающей складками на ягодицах и бедрах. Лицо – «старческое», морщинистое. Подкожно-жировая клетчатка отсутствует даже на лице. Кривая нарастания массы тела плоская или падает вниз. Ткани полностью утрачивают тургор, мышцы атрофичны, но тонус их обычно повышен в связи с расстройствами электролитного баланса и поражением ЦНС. Выражены признаки обезвоживания: жажда, западение большого родничка и глазных яблок, афония, сухость конъюнктив и роговицы, яркое окрашивание слизистой губ, трещины в углах рта («рот воробья»). Температура тела понижена и колеблется соответственно температуре окружающей среды, иногда отмечаются немотивированные подъемы до субфебрильных цифр. Дыхание – поверхностное, аритмичное. Пульс – редкий, слабый, артериальное давление – низкое, тоны сердца приглушены. Живот напряжен, втянут или вздут. Печень и селезенка уменьшены в размерах. Часто отмечаются дискинетические расстройства: срыгивания, рвота, частый жидкий стул. Мочеиспускание редкое, малыми порциями. Вследствие сгущения крови показатели гемоглобина и эритроцитов находятся в пределах нормы или повышены, СОЭ замедлена. В моче большое количество хлоридов, фосфатов, мочевины, иногда обнаруживается ацетон.
Дифференциальный диагноз проводится с синдромом мальабсорбции, наследственными или врожденными энзимопатиями и эндокринными заболеваниями.
Лечение детей с гипотрофией I степени проводится в домашних условиях, а со II-III – в стационаре.
Необходима правильная организация ухода за ребенком (прогулки, теплые ванны, массаж и гимнастика, положительные эмоции).
Основу лечения составляет диетотерапия, которая проводится в три этапа: установление толерантности к пище; этап возрастающих пищевых нагрузок; полное выведение ребенка из гипотрофии.
На первом этапе проводят разгрузку и минимальное кормление. Расчет основных ингредиентов производят таким образом: при I степени белки и углеводы рассчитывают на долженствующую массу тела, а жиры – на приблизительно долженствующую (фактическая + 20% от нее); при II степени – белки и углеводы на приблизительно долженствующую, а жиры – на фактическую; при III все ингредиенты рассчитывают только на фактическую массу.
На втором этапе осуществляется постепенный переход к усиленному кормлению для восстановления резервных возможностей организма. Расчет основных ингредиентов производится таким образом: при I степени белки, жиры и углеводы рассчитывают на долженствующую массу тела; при II степени – белки и углеводы на долженствующую массу, жиры – в начале периода на приблизительно долженствующую, а затем – на долженствующую; при III все ингредиенты рассчитывают только на приблизительно долженствующую, а затем – на долженствующую массу.
Гипостатура
Гипостатура — равномерное отставание ребенка первого года жизни в росте и массе тела, в сравнении со средними нормативными показателями соответствующего возраста. При этом, масса тела для данного роста близка к норме. Однако у таких детей наблюдается удовлетворительное состояние упитанности и тургора кожи.
Длина тела при гипостатуре меньше нормы на 5 — 10 см. (у старших детей на 10 — 20 см.). При этом фактическая масса тела, хотя и меньше средних показателей, пропорционально соответствует росту ребенка.
Причины. Клинические проявления
Частой причиной гипостатуры, является недостаточное количество белка и витаминов, начиная с внутриутробного периода и на первом году его жизни.
Задержка роста чаще всего развивается при:
продолжительной гипотрофии (более 6 мес.)
продолжительных заболеваниях.
Гипостатура может развиться на фоне перенесенной пренатальной (врожденной) дистрофии или длительно текущей недостаточно леченной постнатальной (после рождения) гипотрофии II — III степени. В основе ее возможны нейроэндокринные нарушения. Среди причин развития гипостатуры и гипотрофии, большое значение имеют дефекты ухода за младенцем: дефицит внимания и ласки, психогенной стимуляции (колыбельные, чтение стихов и сказок), отсутствие ежедневных прогулок на свежем воздухе, водных процедур. Клиническая картина:
Внешний вид у детей с гипостатурой необычен, они напоминают недоношенных детей с врожденной гипотрофией, и в это же время отличаются от них.
Это маленькие, но сложенные пропорционально дети. Физически и психически развиваются правильно. Только физические параметры (окружность головы и груди, длина тела стоя и сидя, окружности бедер и голеней, плеча и запястья) не достигают нижней границы нормы. Масса и длина тела у таких детей находится ниже средних возрастных норм или на нижних границах нормы.
Кожа бледная, сухая, тургор тканей снижен, подкожно-жировой слой выражен достаточно. Дети отличаются пониженным аппетитом. Растут медленно. Склонны к частым воспалительным заболеваниям верхних дыхательных путей, к нарушениям обмена веществ, нервным и эндокринным сдвигам; Эмоционально неустойчивы.
Лечение
Включает в себя:
Выявление причин данного состояния, их полное устранение или коррекцию.
Диетотерапию.
Организацию рационального режима, ухода, воспитания, массажа и гимнастики.
Выявление и своевременное лечение очагов инфекции в организме (хронического воспалительного процесса в носоглотке, кариозных зубов), рахита, анемии.
Ферментотерапию (креон, мезим-форте).
Анаболические препараты и витаминотерапию.
Симптоматическое лечение.
Стимулирующая терапия:
Применяют биостимуляторы типа апилака, адаптагены. Проводится лечение рахита, железодефицитной анемии, профилактика и адекватное лечение острых инфекций. При дисбактериозе кишечника применяют бифидумбактерин, линекс, бификол, и др. биопрепараты.
При отсутствии тяжелых заболеваний или пороков развития организма ребенка основу рационального лечения составляет диетотерапия.
Диетотерапия.
Рациональное питание детей должно соответствовать уровню физического развития ребенка (его росту, массе тела). Пищу малыша не следует перегружать белками, жирами, углеводами. Все питательные вещества должны находиться в сбалансированном соотношении, соответственно данному возрасту.
Критерии эффективности диетотерапии:
Улучшение эмоционального статуса (ребенок становится более активным, у него хорошее настроение).
Нормализация аппетита.
Улучшение состояния кожи.
Приобретение новых навыков психомоторного развития.
Ежедневное увеличение массы тела.
Улучшение переваривания пищи (по данным копрограммы).
В случае появления признаков снижения переносимости пищевых продуктов, объем питания временно уменьшают. Следует отметить, что для каждого ребенка необходим индивидуальный подход к диете и темпам ее расширения. Со временем после исчезновения причины заболевания при удовлетворительных условиях и полноценном питании у ребенка быстро восстанавливается внешний вид: цвет кожных покровов, жировой и подкожно-жировой слой, тургор тканей.
При перенесении гипотрофии постепенно увеличивается масса тела.
А длина тела если и повышается, то значительно медленнее. И приобретенное отставание массы тела и роста ребенка от средних нормативных показателей при пропорциональности между ними является признаком гипостатуры.
Паратрофия
Паратрофия — представляет собой заболевание, характеризующееся избытком веса у ребенка. Это следствие хронического нарушения вскармливания малышей первого года жизни, который, в сравнении с установленными нормами, имеет увеличенную массу тела.
У детей паратрофия встречается в возрасте до 3-х лет, особенно если масса тела выше нормативных данных на 10% и более.
Степени паратрофии:
Паратрофия 1 степени: величина превышения массы тела составляет 11-12%
Паратрофия 2 степени: масса тела превышает на 21-30%
Паратрофия 3 степени: масса тела увеличена на 31% и более.
Причины. Симптомы заболевания
Беспорядочное кормление,- частое кормление, которое провоцирует нарушение усвоения пищи,- такие метаболические дефекты, как нарушения обмена аминокислот, болезни накопления,- малая подвижность,- недостаточное пребывание на свежем воздухе,- может быть повышение соматотропного гормона гипофиза, инсулина, задержка в организме лишнего количества воды и прочее.
Симптомы:
бледность кожных покровов,
избыточное откладывание жира в подкожно-жировой клетчатке,
снижение тонуса мышц, упругости тканей,
возможны проявления рахита,
частые аллергические реакции,
ребенок выглядит откормленным и не в меру упитанным,
нередки проблемы с работой кишечника: дисбактериоз, запор,
в естественных складках кожи часто наблюдаются опрелости,
ребенок с паратрофией часто обладает характерным телосложением: широкая грудная клетка, короткая шея, округлые формы тела, узкие лопатки.
Диагностика паратрофии
Анамнестические критерии диагностики позволяют обнаружить этиологические и предрасполагающие факторы, отягощённую по ожирению и обменным заболеваниям наследственность: внутриутробный «перекорм», злоупотребление высококалорийными продуктами, высокобелковое питание, перегрузка электролитами, приём калорийной пищи во второй половине дня, малоподвижность ребёнка, нейроэндокринные расстройства. Клинические критерии диагностики: выраженность клинических и лабораторных признаков зависит от тяжести и клинической формы паратрофии.
Синдром обменных нарушений:
избыток массы тела;
нарушение пропорциональности телосложения;
избыточное отложение жировой ткани;
признаки полигиповитаминоза;
бледность;
пастозность кожи;
снижение тургора тканей;
вялость, нарушение сна и терморегуляции.
избирательное снижение (дети плохо едят овощные виды пищи прикормов, иногда мясо) или повышение (отдают предпочтение молочным продуктам, кашам) аппетита;
высокие неравномерные прибавки массы тела (лабильность весовой кривой);
расстройство стула (запоры или разжижение);
признаки функциональных нарушений желудочно-кишечного пищеварения (по данным копрограммы).
Синдром снижения иммунологической реактивности:
склонность к частым инфекционным заболеваниям с затяжным течением; респираторные заболевания нередко рецидивируют, протекают с обструктивным синдромом и выраженной дыхательной недостаточностью.
Лабораторные критерии диагностики:
Анализ крови — анемия.
Биохимическое исследование крови — диспротеинемия, уменьшение содержания глобулинов и относительное увеличение альбуминов, гиперлипидемия, гиперхолестеринемия, извращённый тип сахарной кривой.
Копрограмма:
при молочном расстройстве питания — стул гнилостный, плотный, блестящий (жирно-мыльный), реакция кала щелочная, часто определяется нейтральный жир, мыла, гнилостная микрофлора:
при мучном расстройстве — стул жёлтый или бурый, плотный, обильный (при дисфункции — пенистый, зелёный), реакция кала кислая, часто определяются вне- и внутриклеточный крахмал, микрофлора йодофильная.
Лечение. Принципы диетотерапии
Организация рационального, сбалансированного питания.
Кормление по режиму.
Оптимизация водного режима.
Проведение этапного диетического лечения:этап (разгрузки) предусматривает отмену высококалорийных продуктов и всех видов прикорма. Общий объём пищи соответствует возрастным нормам. Лучший продукт — грудное молоко. После 6 месяцев целесообразно сочетание грудного молока и кисломолочных смесей.
Длительность этапа — 7-10 дней.этап (переходный) длится 3-4 недели. Детям старше 4 месяцев, вводят соответствующие возрасту прикормы, начиная с овощного пюре.этап (минимально-оптимальной диеты) — ребёнок получает все виды прикорма, соответствующие возрасту. Расчёт необходимого количества белка проводят на фактическую массу тела. Потребность жиров, углеводов, калорий — на долженствующую массу тела.
Профилактика паратрофии
Чтобы у ребёнка не развилась паратрофия, нужно правильно вводить прикормы и следить за весом малыша. Следует тщательно соблюдать режим кормления при искусственном или смешанном вскармливании согласно рекомендациям педиатра, наблюдающего ребёнка.
Сестринский процесс при хронических расстройствах пищеварения
Лечение больных гипотрофией должно быть этапным, комплексным, с учетом этиологических факторов и степени расстройств питания.
Оно должно быть индивидуальным, с учетом функционального состояния органов и систем, наличия или отсутствия инфекционного процесса и его осложнений.
Лечение детей раннего возраста с гипотрофией I степени в большинстве случаев проводят в домашних условиях. Путем подробного опроса матери следует выяснить причину заболевания. Чаще всего оно алиментарного происхождения. Введение соответствующего докорма в виде кислых смесей, коррекция питания назначением творога при недостатке белка или увеличение количества углеводов в рационе из расчета на должную массу тела способствуют устранению начавшегося расстройства питания. Необходимо дать рекомендации матери по улучшению ухода за ребенком (прогулки, регулярное проведение гигиенических ванн и др.).
А детей с гипотрофией II и III степени необходимо госпитализировать.
При этом следует предусмотреть помещение больных с гипотрофией в небольшие палаты или полубоксы с тем, чтобы оградить их от лишних контактов с детьми и особенно с больными ОРВИ.
Все дети требуют оптимального режима сна.
При 2 степени гипотрофии необходимо спать 2 раза в день.
При 3 степени — 3 раза в день.
Помещение проветривают, два раза в сутки проводят влажную уборку. Температура должна поддерживаться в диапазоне 25-26 С.
Организуют тщательный уход за кожей и видимыми слизистыми оболочками, подмывают, кожу обрабатывают прокипяченным подсолнечным маслом.
Общие принципы диетотерапии гипотрофии:
. Увеличение частоты кормлений до 7-8-9 (соответственно при гипотрофии 1-2 и 3 степени).
. Принцип двухфазного питания
Период выяснения пищевой толерантности
Период переходного и оптимального питания
Гипотрофия 1 степени.
Период выяснения толерантности длится 1-3 дня.
-й день назначают 1/2-2/3 суточной потребности в пище.
-й день — 2/3-4/5 суточного количества.
-й день полное суточное количество пищи. Расчет питания производится на должную массу тела. При дефиците в пище белка проводится коррекция (сыром, желтком, ацидофильной пастой, белковым энпитом), жира (жировым энпитом, растительным маслом, сливками), углеводов — овощи, фрукты, рафинированные углеводы).
В отдельных случаях назначают панкреатические ферменты, витамины.
Лечение легкой гипотрофии при отсутствии сопутствующих заболеваний проводится в домашних условиях. Гипотрофия 2 степени.
На 1 этапе проводят осторожное индивидуальное кормление:
На 1 неделе расчет питания по белкам и углеводам производится на фактическую массу + 20%, а жиров на фактическую массу. Количество кормлений увеличивают на 1-2 от возрастной нормы.
На 2 неделе 2/3 суточного количества пищи. На 3 неделе соответственно суточной возрастной потребности. В период выздоровления, исходя из массы тела, высчитывают суточную потребность в энергии:
квартал в сутки необходимо 523-502 кДж/кг (125-120 ккал/кг)
квартал 502-481 кДж/кг (120-115 ккал/кг)
квартал 481-460 кДж/кг (115-110- ккал/кг)
квартал 460-418 (110-100 ккал/кг).
При смешанном и искусственном вскармливании энергетическая ценность увеличивается на 5-10%
Гипотрофия 3 степени.
Детей с гипотрофией 3 степени начинают кормить грудным молоком (нативным или донорским). В крайнем случае адаптированными молочно-кислыми смесями.
неделя 1/3 суточной потребности. Число кормлений увеличено на 2-3. 2/3 суточной потребности обеспечивают жидкостью (овощные и фруктовые отвары, электролитные растворы, парентеральное питание.
неделя 1/2 должной суточной потребности в пище.
неделя 2/3/ должной суточной потребности в пище.
Белки и углеводы рассчитываются на должную массу, а жир только на фактическую.
При анорексии, низкой толерантности к пище назначают частичное парентеральное питание — аминокислотные смеси (полиамин, альвезин Новый, амикин, левамин), растворы инсулина с глюкозой 1 ЕД/5 г глюкозы.
Диетотерапия является основополагающим методом лечения при гипотрофии. Назначение соответствующих продуктов питания зависит от множества факторов, в частности от степени истощения организма. Но самым главным в подходе к диетотерапии является степень поражения желудочно-кишечного тракта или центральной нервной системы.
Заключение
Нормальное развитие ребенка находится в тесной связи с деятельностью его органов пищеварения. Расстройство пищеварения приводит к расстройству питания, нарушению обмена, которое нередко сопровождается нарушением функций многих органов и систем.
Медработник первичного звена медицинской помощи занимает уникальное положение, позволяющее рано диагностировать расстройства питания и предотвратить их прогрессирование на ранних стадиях болезни. Первичная и вторичная профилактика включает необходимость скрининга расстройств питания, измерения роста и веса, как рутинной части мероприятий ежегодного наблюдения.
Необходимо уделять пристальное внимание выявлению ранних симптомов расстройств питания. Раннее распознавание и лечение расстройств питания может предотвратить физические и психические последствия нарушений пищеварения, которые приводят к прогрессированию заболевания на поздней стадии. Скрининговые вопросы относительно удовлетворенности внешним видом своего тела должны задаваться всем детям препубертатного возраста и подросткам. Вес и рост должно определять регулярно (предпочтительно в больничном платье, т.к. для увеличения веса могут быть использованы различные предметы). Полученные данные относительно роста и веса должны вноситься в педиатрические карты роста, для того чтобы определить их задержку, связанную со сниженным употреблением нутриентов.
Большое значение имеет организация ухода, ребенка с хроническим расстройством питания не столько лечат, сколько выхаживают. Очень важно создавать у ребенка положительный эмоциональный тонус — необходимо чаще брать его на руки (профилактика гипостатических пневмоний), разговаривать с ним, гулять.
Методическая разработка для студентов
Тема: «ХРОНИЧЕСКИЕ РАССТРОЙСТВА ПИТАНИЯ (дистрофии)»
Продолжительность занятия — 4 часа Основные вопросы темы:
1. Понятие и виды хронических расстройств питания;
2. Причины и предрасполагающие факторы в развитии дистрофий;
3. Классификация;
4. Патогенез пренатальной, постнатальной гипотрофии;
5. Клиника различных видов гипотрофии;
6. Понятия гипостатуры, паратрофии, квашиоркора;
7. Диагностика дистрофий, современная диагностика гипотрофии плода;
8. Дифференциальный диагноз дистрофий;
9. Диетотерапия гипотрофии;
10. Медикаментозное лечение;
11. Профилактика развития дистрофий.
Дополнительный материал
1. Экссудативно-катаральный диатез;
2. Аллергический диатез;
3. Лимфатико-гипопластический диатез;
4. Нервно-артритический диатез.
Цель занятия:
Студент должен изучить клинические проявления, принципы терапии и профилактики хронических расстройств питания и аномалий конституции.
Студент должен знать и уметь:
1. Оценить состояние питания, физическое и психомоторное развитие ребенка.
2. Оценить правильность получаемого ребенком питания и при необходимости произвести коррекцию.
3. Диагностировать гипотрофию и выявить причины ее развития.
4. Рассчитывать питание в зависимости от степени гипотрофии и этапа лечения.
5. Уметь дифференцировать различные проявления диатезов.
6. Составлять план профилактических мероприятий диатезов.
Оснащение занятия:
Схема истории болезни, микротаблицы, макротаблипы, слайды, видеофильм, тематические больные, муляжи лекарственных препаратов.
Методические указания по теме
Хронические расстройства питания (.дистрофии) — развиваются
преимущественно у детей раннего возраста и характеризуется нарушением усвоения питательных веществ тканями организма.
Различают следующие виды дистрофии:
1) дистрофия с дефицитом массы тела (гипотрофия);
2) дистрофия с массой тела, соответствующей росту (паратрофия);
3) дистрофия с избыточной массой тела (ожирение).
Частота встречаемости дистрофии, особенно гипотрофии, зависит от социально — экономического уровня развития той территории, в которой находятся дети. По данным ВОЗ, в высокоразвитых странах гипотрофия встречается достаточно редко — у 0.5 — 1% детей раннего возраста, и только в легкой форме. В
странах с развивающейся и отсталой экономикой этот показатель достигает 10-20% и более.
Этиология гипотрофий
По времени возникновения различают врожденные (пренатальные) приобретенные (постнатальные) гипотрофии. При группировке причин пренатальной гипотрофии по топографнческому признаку выделяют:
1. Преплацентарные (природные и скулатные) факторы — возраст матери, ее телосложение, паритет, осложнение беременности, заболевания матери, хронические интоксикации (лекарственные, профессиональные, алкоголь, курение).
2. Плацентарные (пуповинные) причины — тромбозы, гематомы, гемангиомы, инфаркты, предлежание и гипоплазвя цлаценты, аномалии развития пуповины.
3. Постплацентарные причины — врожденные уродства, внутриутробные
заболевания плода.
Причины возникновения постнатальной гипотрофии делят на 2 группы. А. Экзогенные причины
1) Алиментарные факторы: количественный недокорм (гипогалактия, назначение недостаточного количества смесей при искусственном вскармливании, качественный недокорм (бедность белками или жирами женского молока при неправильном питании кормящей матери, позднее или ранее введение прикорма, кормление смесями или продуктами не соответствующими по содержанию белков или жиров возрастным потребностям ребенка, неправильное приготовление смесей, бедность пищи витаминами).
2) Инфекционные факторы: внутриутробные инфекции; иифекционные заболевания первых месяцев жизни желудочно-кишечного тракта, частые острые инфекции, пиелонефрит, сепсис и т.д.
3) Токсические факторы: гипервитаминозы (особенно часто гипервитаминоз Д, лекарственные отравления и др.
4) Недостатки ухода, режима, воспитания.
Из экзогенных факторов одной из наиболее частых причин гипотрофии являются инфекционные заболевания желудочно-кишечного тракта. Поражение кишечника при позднем или нерациональном лечении приводит к нарушению всасывания пищевых веществ, угнетению ферментативной активности желудка и кишечника, развитию дискинезии жедудочно-кишечного тракта и дисбактериоза, которые способствуют прогрессированию или формированию гипотрофии. В. Эндогенные причины гипотрофии (вторичной, симптоматической) могут
быть:
1) Пороки развития желудочно-кишечного тракта (пилоростеноз, мегаколон, атрезия желчных путей и др.) пороки сердца, почек, печени, головы, мозга, диафрагмальная грыжа и др.
2) Наследственные аномалии обмена веществ,
3) Синдром мальабсорбции.
4) Врожденные или приобретенные поражения ЦНС.
5) Наследственные иммунодефицитные состояния.
6) Эндокринологические заболевания (сахарный диабет, врожденная дисплазия
надпочечников с синдромом потери солей и др.).
При тщательном сборе данных анамнеза, как правило, устанавливают смешанную этиологию гипотрофии у ребенка. Особенно часто диагностируются алиментарно-инфекционная этиология гипотрофии на фоне таких предрасполагающих факторов, как неблагоприятное течение внутриутробного периода развития, рахит, анемия, дефекты ухода.
Патогенез гипотрофии ( см. приложение 2)
А. Пренатальная гипотрофия
В зависимости от силы и продолжительности воздействия вредного фактора, в плаценте возникают расстройства кровообращения, нарушающие основные обмены между матерью и плодом. В организме плода развивается гипоксия, ведущая к нарушению окислительных процессов и усугубляющих нарушение всех видов обмена веществ. Это сказывается на массе и росте, что приводит к функциональной незрелости плода. Вследствие расстройства кровообращения, повышается чувствительность плода к родовым травмам и к функциональным нарушениям ЦНС. Дети имеют пониженные показатели физического развития, не соответствующие сроку беременности, недостаток массы, по сравнению с нормальными показателями может варьировать от 200 до 900 г.
В силу этого подкожный жировой слой выражен недостаточно или совершенно отсутствует. Реже обнаруживают отставание в росте. Отмечается большая физиологическая убыль в массе (более 10-15%) и замедленное восстановление первоначального веса, более позднее заживляется пупочная ранка, вследствие снижения темпов репаративньк процессов. В. Постнатальная гипотрофия
Под влиянием этиологических факторов изменяется прежде всего нормальная функция желудочно-кишечного тракта. Это проявляется в снижении кислотности желудочного сока, снижении ферментативной активности желудка (синтеза пепсина, парапепсина — пепсина В, химозина) и кишечника, что приводит к
уменьшению всасывания пищевьк веществ в желудочно-кншечном тракте замедлению эвакуаторной функции желудка и кишечника. Вследствие этого понижается толерантность к пище, в кале больного увеличивается содержание белков, жиров и углеводов. Адекватная возрастная пищевая нагрузка для ребенка с гипотрофией II и III степени может вызвать острое расстройство пищеварения —
диспепсию.
Нарушение правильного чередования приемов пищи, недостаточное введение или избыточное количество какого-либо пищевого ингредиента приводит к язменению чувствительности центров голода и насыщения к рефлексогенам, что проявляется дисфункцией коры головного мозта в виде понижения, а затем исчезновения не только условных, но даже и безусловных рефлексов на кормление Нарастает анорексия и формируется отрицательный рефлекс к пище.
.Расстройства ЦНС усугубляют дисфункцию внутренних органов: нарушается моторнка кишечника, возникает одышка, аритмия сердца, уменьшается глубина дыхания и др.
У больных гипотрофией снижается функциональная активность поджелудочной жепезы (уменьшается актнвносгь протеаз и карбокснполипептида, амилазы и липазы); печени (нарушаются процессы дезаминирования,
антитоксическая, белково-синтетическая. углеводная и др. функции); сердца (приглушение тонов сердца, трофические изменения сердечной мышцы, замедление скорости коронарного кровотока); легких (гипоксемия вследствие метаплазии альвеолярного эпителия в многослойный, гемодянамнческие нарушения в легких, центральные нарушения ритма дыхания); почек (полиурия, поллакиурия, при тяжелых формах гипотрофии — азотемия, нефросклероз кроветворной системы (анемия, лнмфопення). В патогенезе анемии у больных гипотрофией ведущее значение имеет дефицит железа, меди. белков аминокислот, вигаминов B6, В12.
По мере прогресснрования гипотрофии увеличивается функцнональная недостаточность желез внутренней секреции (надпочечников, щитовидной железы, тимуса, гипофиза), т.е. возникает плюригландулярная недостаточность (псевдогипофнзэктомия)
В обмене веществ: белкового (катаболическая направленность, амнноацндурия, гипопротеинемия, диспротеинемия со снижением уровня альбумина), углеводного (гипоглнкемия, плоские сахарные кривые, гпюкозурия, накопление в крови недоокисленных продуктов, молочной кислот, как следствие усиления гликолиза, что ведет к ацидозу), жирового (гипохолестеринемия, гиперлипидэмия, так как снижена лнполнтическая активность сыворотки, гиполипопротеинемия), минерального (обезвоживания, деминерализация костей, гипокалиемия, пгипонатриемия, гипофосфатемня), КОС (уменьшение мощности буферных оснований крови, метаболический ацидоз), полнгиповитаминоз.
Нарушается терморегуляция (усиление теплоотдачи из-за увеличения поверхности тела на единицу массы тела н уменьшения химической теплопродукции).
Если при гипотрофии I степени иммунологическая активность существенно не изменена, то при гитотрофиях II и III степени уменьшается активность как неспецифической, так н специфической защиты, что способствует наслоению
инфекции. У детей с гипотрофией, вследствие иммунной гало- и анэргии, ннфекционньцй процесс протекает малоснмпгомно, латентно.
КЛАССИФИКАЦИЯ ХРОНИЧЕСКИХ РАССТРОЙСТВ ПИТАНИЯ У ДЕТЕЙ РАННЕГО ВОЗРАСТА
Г И. Зайцева с соавт.. 1982
|
Тип дистрофии по отношению к длине и массе тела |
Степень тяжести |
Период |
Происхождение |
Этиология |
|
|
Экзогенная |
Эндогенная |
||||
|
Гипотрофия (отставание массы тела от роста) Гипостатура (равномерное от ставшие в массе тела и росте) Паратрофия а) с преобладанием массы тела над ростом; б) с равномерными избыточными масой и ростом; в) с неравномерными массой тела и ростом |
I Дефицит массы 10-20% II Дефицит массы 20-30% III дефицит массы >30% |
Начальный Прогрессирования Стабилизации Реконвалесценции |
Пренатальное Постнатальное Пренатально -постнатальное |
Алиментарная (недокорм, перекорм, несбалансированное питание и т.д.) Инфекционная Токсическая Нарушение режима, дефекты воспитания и др. неблагоприятные факторы |
Аномалии конституции (диатезы), эндокринные и нейроэндокринные расстройства Пороки развития Первичные (наследственные и врожденные) энзимопатии: а) первичные нарушения расщепления и всасывания б) наследственная патология обмена веществ Иммунодефицитные состоявия и заболевания |
|
Смешанная: экзогенная, эндогенная |
|||||
Дополнение к разлялу «Дистрофии зндогенной этиологии»
1 Диатезы: экссудативньй, лимфатический, нервно-артритический.
2 Эндогенные и нейроэндокринные расстройства: гипотиреоз, адреногенигапьный сивдром, гипофизарный нанизм, аномалии випочковой железы и др.
3. Пороки развития: центральной нервной системы, сердечно-сосудистой, желудочно-кишечного тракта (долихосигма, атрезия жепчных ходов и др.)
4. Первичные нарушения всасыааяия, мальабсорбции: недостаточность всасывания глюкозы, галактозы, белков к др.
5. Экссудатавные энтеропатия, целиакая, липопротеинемия, муковисцидоз и др. 6 Первичные нарушения обмена веществ:
—аминокислотного: фенилкетонурия, гомоцистинурия и др.
—углеводного — галактоземия, фруктоземия и др
—жирового — ксантоматоз, внутриклеточный липоидоз.
Дополнение к разделу «Дистрофии пренатального происхождения»
Форма пренатальной дистрофии по Фатеевой Е.М: невропатическая, нейроднстрофическая, нейроэндокринная, энцефалопатическаяя.
Клинико-диагностические признаки гипотрофии у детей
|
Осяовяыв клммшесхие |
1 степень |
П сгепоиь |
Шствяень |
|
симптомы |
|||
|
1. Нарушении пягаяяя |
|||
|
1. Дефицт массы тела во |
|||
|
отношению: |
|||
|
*) к долженствующей |
10-20% |
20-30% |
Более 30% |
|
к» сев |
|||
|
б) 11 росту |
от 0,5 до 1,5о |
от 1,5 до 2в |
Бопве2в |
|
от Pa до Рю (во |
отРиДоР, |
НИЖвР> |
|
|
п«рцсвт таб.-ащм) |
|||
|
2. Трофячсскмо кзмененйх |
Умсрсини бледная, |
Бледя»*, сухая. У |
То же, что при В |
|
кожи |
со сниженной |
новорожденных — |
стгогаи |
|
эластячностыо. |
иласгинчятое |
||
|
огрубелмдвое |
|||
|
шсяувкмяе кожи: |
|||
|
опропоетм, трещины, |
|||
|
чтиов-теня», |
|||
|
3. Истонченис поджожлого |
Умеренное |
Отчетливое, на |
Зшчмтслыюе. |
|
слоя. |
(пивным образом на |
животе, туловище, |
Отчетливо |
|
животе, туловище и |
конечноеих. |
контурируютсв |
|
|
консчяостж). |
Умеренно |
ребра и сустары. |
|
|
коятурнруютсв |
|||
|
4. Снижение тургора |
Умеренное, на |
ребра, сусивы. |
Ремюе |
|
ткнией |
кояечмостю. |
Отчетлавое. |
|
|
Дрибяыв складхх |
|||
|
кожя яд |
|||
|
конечностях, шее. |
|||
|
5. Индекс Чутапкой |
10.15 |
Уменьшение |
Отрнцатсяьнмв |
|
мышечной Mieeu. |
|||
|
2-10 |
|||
|
П. 1Ьп«яекмн |
|||
|
фу»1КЦИ Потеря аппетита у ребенка
Профессор Карпов Владимир Владимирович — Доктор медицинских наук, врач — педиатр высшей квалификационной, заведующий кафедры детских болезней РостГМУ, автор различных методик и научных трудов. Профессор Чепурная Мария Михайловна — Доктор медицинских наук, Заслуженный врач Российской Федерации, Заведующая пульмонологическим отделением ГУЗ «Областная детская больница, г. Ростов-на-Дону Андриященко Ирина Ивановна — врач педиатр высшей квалификационной категории. Книга: «Заболевания детей раннего возраста». (Карпова В.В.) Потеря аппетита у ребенка — хронические расстройства питания у детей. Определение Хронические расстройства питания, часто обозначаемые термином «дистрофия» — это патологическое состояние, характеризующееся нарушениями физического развития, метаболизма, иммунитета, морфофункционального состояния внутренних органов и систем организма в результате недостаточного или избыточного поступления и/или усвоения питательных веществ. Диагностика хронических расстройств питания в основном базируется на оценке упитанности ребенка. В зависимости от характера нарушения трофики выделяют следующие типы дистрофии по соотношению массы и длины тела: • гипотрофия — это хроническое расстройство питания, характеризующееся отставанием массы тела от роста в результате прекращения нарастания массы тела, нарушением трофических функций организма, пищеварения, обмена веществ, задержкой нервно-психического развития, снижением специфических и неспецифических сил организма в следствии белковоэнергетического голодания; Наибольшую опасность для состояния здоровья и качества жизни ребенка представляет гипотрофия в результате неблагоприятного влияния на физическое и нервно-психическое развитие, иммунологическую реактивность, снижение толерантности к пище. Диагноз «гипотрофия» правомочен у детей первых лет жизни, так как это связано с анатомо-физиологическими особенностями растущего организма. В первые месяцы жизни ребенка желудочно-кишечному тракту приходится переваривать относительно большее количество пищи, а интермедиарный обмен веществ требует очень интенсивных процессов ретенции и ассимиляции. Вместе с тем в функциональном отношении как желудочно-кишечный тракт, так и другие органы, в частности печень, ещё относительно несовершенны, обладают незначительной резервной возможностью и ограниченной толерантностью к пище. Поэтому легче и быстрее наступает извращение их функции при предъявлении к ним повышенных требований. С другой стороны, для ребенка раннего возраста характерно несовершенство нервно-рефлекторных механизмов, осуществляющих регуляцию всех видов обмена, худшее развитие компенсаторных реакций организма и адаптации ребенка к изменениям внешней среды. В России долгие годы был общепринятым термин гипотрофия, что является синонимом белково-энергетической недостаточности, используемый в зарубежной литературе и рекомендованный в МКБ -10. Белково-энергетическая недостаточность (БЭН) — это алиментарно-зависимое состояние, вызванное достаточным по длительности и/или интенсивности преимущественно белковым и/или энергетическим голоданием, проявляющееся дефицитом массы тела и/или роста и комплексным нарушением гомеостаза организма в виде изменения основных метаболических процессов, водно-электролитного дисбаланса, нарушения нервной регуляции, эндокринного дисбаланса, угнетения иммунной системы, дисфункции желудочно-кишечного тракта и других органов и систем. Распространенность Точных сведений о распространённости гипотрофии у детей в России нет, так как легкие и средне-тяжелые её формы регистрируются не всегда. Тяжелая степень гипотрофии диагностируется у 1-2% детей раннего возраста. В странах с низким экономическим уровнем этот показатель составляет 10-20%. В тоже время пренатальная гипотрофия наблюдается у 10-20% доношенных новорождённых и до 25% у недоношенных. Классификация хронических расстройств питания у детей раннего возраста (Г.И.Степанова, Л.А.Строгонова, 1981) 1. По времени возникновения: 2.Этиология Экзогенная: Эндогенная: 3. По степени тяжести: 4. Период заболевания: Пренатальную гипотрофию, в соответствии с указаниями Е.М.Фатеевой, подразделяют на невропатическую, нейродистро- фическую, нейроэндокринную и энцефалопатическую. Следует отметить, что в последние годы возросла диагностика пренатальной гипотрофии у детей. Данные статистики свидетельствуют о том, что до 20% новорождённых рождается с признаками пренатальной гипотрофии. О пренатальной гипотрофии следует говорить в тех случаях, когда при доношенной беременности рождается ребёнок с массой менее 2800 г и длиной более 48 см. У недоношенных детей необходимо использовать оценочные таблицы массы тела недоношенного с учётом его длины относительно сроков гестации (Г.М.Дементьева, 1981). Этиология — потеря аппетита у ребенка. Причины развития пренатальной гипотрофии достаточно многочисленны. Условно их можно разделить на три группы: преплацентарные, плацентарные и постплацентарные, которые чаще всего характеризуются задержкой внутриутробного развития плода (ЗВУР). К первой группе следует отнести конституциональные особенности матери, соматические заболевания, гестозы, недостаточное питание матери, неблагоприятные социально-экономические и экологические условия, вредные привычки, возраст матери. Плацентарные причины обусловлены тромбозом, наличием гематом и инфарктов плаценты, её гиперплазией, кальцинозом, фиброзом, плацентитом. Третья группа причин (постплацентарные) обусловлена аномалиями пуповины, много-плодной беременностью, внутриутробными инфекциями, врожденными пороками развития плода, хромосомными заболеваниями и моногенным синдромом. Из общего числа детей с гипотрофией, последняя у 66% развивается в первом полугодии, у 20% — во втором полугодии и только у 10% на втором году жизни. Причинами постнатальной гипотрофии могут быть экзогенные и эндогенные факторы. Из экзогенных факторов наиболее частым является алиментарный. Это связано с большой распространенностью гипогалактии у матерей, аллергии у детей, что может быть причиной количественного недокорма. Немаловажную роль в развитии гипотрофии играют и качественные нарушения питания ребенка: дефицит витаминов, недостаток или избыток какого-либо пищевого ингредиента (белков, жиров, углеводов). Так, при повышенной белковой нагрузке, особенно на фоне недостатка углеводов, снижается его утилизация, накапливаются азотистые продукты обмена, аминокислоты, аммиак, возникает ацидоз, что приводит к появлению дистрофических изменений в мозговой ткани и паренхиматозных органах. Злоупотребление кашами может стать причиной так называемого мучного расстройства питания, которое проявляется в виде паратрофии, либо гипотрофии. Особое внимание следует уделять предупреждению у ребенка неврогенной анорексии, развивающейся в результате насильственного кормления, частой и необоснованной смены блюд. Нередко у детей отмечается ухудшение аппетита в результате длительного и массивного приема лекарств, излишнего употребления сладостей. Немаловажную роль в возникновении гипотрофии играют острые и хронические инфекции, особенно желудочно-кишечного тракта. Поражения кишечника при позднем или неадекватном лечении приводит к нарушению всасывания питательных веществ, угнетению ферментативной активности желудка и кишечника, развитию дисбактериоза, которые способствуют формированию или прогрессированию гипотрофии. Одной из причин расстройства аппетита и трофических функций организма является неправильная организация ухода, режима и воспитания ребенка. Наиболее тяжелые варианты постнатальной гипотрофии развиваются при воздействии эндогенных факторов. Из которых следует выделить прежде всего пороки развития ЖКТ (атрезии, пилоростеноз, расщелины мягкого и твердого неба), сердца и сосудов, синдром мальабсорбции и наследственные нарушения обмена веществ (фенилкетонурия, цистинурия, галактоземия, ксантоматоз и др.), эндокринные и нейроэндокринные расстройства, тяжелые поражения ЦНС, иммунодефицитные состояния. Аномалии конституции сами по себе не вызывают развитие гипотрофии, но при воздействии вышеперечисленных факторов быстрее развивается снижение толерантности к пище, нарушение обмена веществ, что ведет к формированию хронического расстройства питания. Учитывая все вышеизложенное, следует указать, что этиология гипотрофий достаточно разнообразна, часто имеет место сочетание пренатальных и постнатальных, экзогенных и эндогенных факторов. Однако в настоящее время причины сугубо алиментарного характера не занимают ведущего положения. Чаще имеют место дефекты в режиме питания. В связи с этим внимание педиатров должно уделяться вопросам организации правильного и рационального питания детей, находящихся на смешанном и искусственном вскармливании. Наиболее тяжелые и прогрессирующие варианты гипотрофии у детей наблюдаются при сочетании пренатальной гипотрофии с воздействием эндогенных факторов. Поэтому в случаях упорной, неподдающейся лечению гипотрофии необходимо проводить дифференциальную диагностику с целью исключения тех врожденных и наследственных заболеваний, при которых гипотрофия является одним из постоянных симптомов. Патогенез Патогенез хронических расстройств питания имеет свои особенности в зависимости от этиологически значимых факторов. В развитии пренатальной гипотрофии главную роль играют нарушения маточно-плацентарного кровообращения и внутриутробная гипоксия плода, характеризующиеся достаточно выраженными эндокринными и метаболическими изменениями и проявляющиеся хронической стрессовой реакцией. Последняя у плода и новорожденного с пренатальной гипотрофией обусловливает гиповолемию, централизацию кровообращения и гипердинамиче скую реакцию миокарда, гипогликемию, уменьшение содержания гликогена в печени и сердце, гипокальциемию и гипомагнемию, метаболический ацидоз, накопление продуктов перекисного окисления липидов и повышение уровня гематокрита, гиперкоа- гуляционный синдром, нарушение микрогемоциркуляции, возникновение иммунодепрессии. Патогенез постнатальной гипотрофии может быть представлен как единый патофизиологический процесс, сопровождающийся глубокими нарушениями всех видов обмена, изменениями со стороны внутренних органов и, прежде всего, со стороны органов пищеварения, нарушении возбудимости коры головного мозга, а также сниженииЙ/шмунологической реактивности организма. В результате неадекватного питания или воздействия других предрасполагающих факторов изменяется и извращается нормальная функция желудочно-кишечного тракта. Это выражается в снижении активности ферментов желудка, поджелудочной железы, кишечника, ухудшается полостное и мембранное пищеварение, всасывание конечных продуктов в кишечнике. Все это ведет к нарушению секреторной, моторной и всасывательной функции желудочно-кишечного тракта, усилению гнилостных и бродильных процессов в кишечнике. Вследствие этого снижается толерантность к пище и создаются благоприятные условия для развития дисбактериоза кишечника. По мере прогрессирования заболевания происходит снижение возбудимости коры головного мозга, приводящее к дисфункции подкорковых образований и исчезновению в дальнейшем не только условных, но и безусловных рефлексов. Все это вызывает понижение аппетита и развитие у ребенка отрицательного рефлекса к пище и даже рвоту. Качественное и количественное голодание неизбежно обусловливает недостаточное поступление в организм пластического и энергетического материала, что влечет за собой извращение всего ферментативного аппарата крови и обмена веществ. В основе любой по генезу гипотрофии лежит расстройство в той или иной степени белкового, жирового, углеводного, водно-минерального, энергетического и витаминного обмена. Нарушение процессов ферментативного расщепления пищи ведет к снижению ферментативной активности крови, нарушению антитоксической, дезаминирующей, гликоген- и протромбин образовательной функции печени. В процессе распада белков образуются промежуточные токсические вещества, которые еще больше ухудшают обменные процессы, усиливают интоксикацию, увеличивают расход витаминов, извращают деятельность всей гуморальной системы. Ферментативные пути окисления жира замещаются неферментативным свободнорадикальным окислением липидов, что сопровождается накоплением в организме перекисных радикалов, оказывающих общетоксическое действие, повреждение мембран и органоидов клеток. При внешнем и внутреннем голодании организм для поддержания своих жизненных процессов, для сохранения основного обмена затрачивает собственные запасы углеводов, жиров, белков. Первое время организм использует запасы жира и гликогена подкожно-жировой клетчатки, мышц, внутренних органов, а в дальнейшем и клеток паренхиматозных органов. В этот период в результате резкого снижения иммунологической реактивности развивается состояние дизергии, при котором легко возникают токсико-септические состояния, нередко приводящие к летальному исходу. Таким образом, при тяжелой степени гипотрофии развитие метаболического ацидоза, эндогенного токсикоза, нарушение функции практически всех органов и систем следует рассматривать как «катастрофу обмена». Клиника При экзогенной (первичной) гипотрофии диагноз гипотрофии выносится как основное заболевание, тогда как при эндогенной (вторичной) ставится диагноз основного заболевания, а гипотрофия расценивается как осложнение. Обычно ребенок с гипотрофией по своим внешним признакам сопоставляется с нормально развивающимся ребенком, т. е. нормотрофиком или эйтрофиком. Согласно указаниям Г.Н. Сперанского под термином «нормотрофия» следует понимать «не только нормальную упитанность ребенка, но и адекватную функцию всех органов и систем организма и динамически правильное его раз витие». Если у ребенка имеются те или иные отклонения от этих показателей, то они присущи ребенку, страдающему дистрофией. Оценка состояния питания ребенка слагается из внешнего осмотра, определения его массы, роста соответственно возрасту и других показателей физического развития, тонуса и эластичности кожных покровов, оценки температурной кривой, состояния иммунитета. Еще раз следует подчеркнуть, что для диагностики гипотрофии степень отставания массы тела от роста имеет важное, но не основное значение. Серьёзность расстройств питания ребенка больше всего характеризует глубина регуляторных функциональных и обменных нарушений, которые находят свое отражение в общих симптомах заболевания. При гипотрофии 7 степени дефицит массы колеблется от 10 до 20% или в пределах Р25 — Р10 по центильным таблицам. Имеет место некоторое истончение подкожно-жирового слоя на животе, грудной клетке, бедрах, снижение эластичности кожи и тургора тканей, повышенная нервная возбудимость. Кривая массы уплощена, длина тела и психомоторное развитие соответствует возрасту. Секреторная функция ЖКТ в норме, дисбактериоза нет или 1 степени. При гипотрофии 2 степени дефицит массы тела относительно возрастной нормы составляет от 21 до 30% или в пределах от Р10 до РЗ по центильным таблицам. Подкожно-жировой слой еще больше уменьшается на животе, истончается на других участках туловища и конечностей, но сохраняется на лице. Тургор тканей значительно снижен, тонус мышц понижен. Кожа бледная с сероватым оттенком, сухая, легко собирается в складки, особенно на внутренней поверхности бедер. Имеются признаки полигиповитаминоза, аппетит и толерантность к пище снижены. Психомоторное развитие ребенка задерживается, нарушается терморегуляция, в результате снижения иммунитета часто присоединяются интеркуррентные заболевания, развивается дисбактериоз 1-2 степени. Самочувствие нарушается, ребенок становится вялым, иногда раздражительным, нарушается ритм сна. При гипотрофии 3 степени дефицит массы тела составляет более 30% или менее РЗ по центильным таблицам, кривая массы тела имеет тенденцию к снижению, отмечается отставание в росте. Подкожно-жировой слой практически отсутствует, иногда заметен на щеках. Кожа бледная с сероватым оттенком, морщинистая, легко собирается в складки и с трудом расправляется, местами шелушится, на ягодицах и мошонке могут быть язвочки трофического характера. На спине и конечностях нередко отмечается гипертрихоз. На вздутом животе кожа натянута, блестящая, с отчетливо выраженным сосудистым рисунком, иногда контурируются петли кишечника. Кожа на лбу и щеках собрана в складки, нос, скулы, подбородок заостряются, глаза кажутся большими и запавшими, выражение лица старческое. Мышцы атрофированы, тонус их повышен. Температура тела понижена до 36 — 35° и колеблется в зависимости от температуры окружающей среды, временами отмечаются подъёмы до субфебрильных цифр. Выражены признаки эксикоза: жажда, западение большого родничка и глазных яблок, афония, сухость конъюнктивы и роговицы. Ребенок безразличен к окружающему, иногда капризен, почти всегда жадно пьёт воду, аппетит чаще снижен или отсутствует, плач и крик слабые, монотонные. Дыхание поверхностное с удлиненным выдохом, периодическими остановками. Тоны сердца приглушены, брадикардия, снижение артериального давления. Резко выражены признаки полигиповитаминоза, вследствие снижения иммунитета часто присоединяются интеркуррентные инфекции с исходом в токсико- септические состояния, дисбактериоз 3 степени. В ряде случаев может развиваться отёчно-дистрофическое состояние, подобное квашиоркору. Квашиоркор — это тяжелая форма алиментарной дистрофии у детей раннего возраста, развивающаяся в результате белкового голодания при относительной недостаточности углеводов и характеризующаяся задержкой физического и психомоторного развития, распространенными отеками, нарушением пигментации кожи и волос, кишечного всасывания при сравнительной сохранности подкожно-жирового слоя. Характерна тетрада Джелифа: безбелковые отеки, отставание в физическом развитии (масса снижается более чем на 30%), мышечное истощение, изменение психики. В иностранной литературе при описании хронических расстройств питания у детей достаточно часто используются термины: «алиментарный маразм», «атрофия», «атрепсия», «декомпозиция». Маразм в переводе с греческого означает угасание, истощение. Этоттермин может быть использован при хронических расстройствах питания у детей более старших возрастных групп при критическом дефиците массы тела более 30-50%. Ведущее значение в развитии этого синдрома имеет не только значительная белково-энергетическая недостаточность, но и тяжёлые хронические заболевания, особенно желудочно-кишечного тракта. Термин «атрофия» указывает на тяжелое хроническое расстройство питания (^потрофия 3 степени) у детей первых лет жизни. В тех случаях, когда отсутствует возможность переваривать и всасывать необходимые для жизнедеятельности детского организма питательные вещества используется термин «атрепсия». Тогда как при потере возможности построения тканей — термин «декомпозиция». Диагностика Основными критериями диагностики гипотрофии у детей наряду с анамнезом, данными объективного исследования являются результаты параклинических исследований. Картина крови при гипотрофии различна. Обычно имеет место анемия гипохромного характера. При тяжёлых формах гипотрофии в сочетании с нарушениями водно-электролитного обмена может иметь место сгущение крови, в результате чего повышается количество эритроцитов и гемоглобина, увеличивается показатель гематокрита. Более значительные изменения отмечаются со стороны показателей, характеризующих обмен веществ: белковый обмен — гипо- и диспротеинемия; жировой обмен — гипохолестеринемия, гипопротеинемия; углеводный обмен — гипогликемия; минеральный обмен — эксикоз, метаболический ацидоз, деминерализация костей, гипокалиемия, гипофосфатемия, гипонатриемия, дефицит железа, аминоацидемия. Формирующееся вторичное иммунодефицитное состояние характеризуется нарушениями клеточного и гуморального иммунитета, снижением фагоцитарной и бактерицидной активности нейтрофилов и макрофагов. Лечение Лечение детей с гипотрофией зависит от вида белковоэнергетической недостаточности, степени её тяжести и направлено на устранение этиологически значимых причин и нормализацию нарушенных функций организма. Общий план лечения может быть представлен следующим образом: Базисной терапией гипотрофии является диетотерапия, которая должна проводиться с учётом следующих положений: Выделяют следующие этапы диетотерапии: разгрузки (3-5 дней), минимального питания (3-5 дней), промежуточный (5-7 дней) и оптимального или усиленного питания до восстановления возрастной долженствующей массы тела ребенка. Этап разгрузки по объёму и характеру пищи преследует следующие цели: определение толерантности к пище, урегулирование водноминерального и межуточного обмена, адаптация ребёнка к постепенному увеличению объёма пищи и обеспечение энергией основного обмена. Этап минимального питания предусматривает дальнейшее повышение объёма пищи от уровня, обеспечивающего основной обмен, до полной суточной потребности на фактическую массу, при которой определённая часть пищевых веществ может использоваться в пластических целях. При достаточной толерантности этап разгрузки и минимального питания объединяются в адаптационный период продолжительностью не более 3-5 дней. Задача промежуточного этапа — постепенная адаптация пи-щеварительной системы и обмена веществ ребёнка не только к возрастному объёму питания, но и к постепенному увеличению в достигнутом объёме пищи вначале содержания белка, а затем углеводов и жиров до долженствующих возрастных потребностей на кг массы тела. На этапе оптимального (усиленного) питания достигается полное обеспечение потребности больного ребёнка в пищевых веществах, энергии и такому соотношению пищевых ингредиентов, которое обеспечивало бы максимальное их усвоение и устранение имеющегося дефицита массы тела. На оптимальном этапе диетотерапии больных с первичной гипотрофией дополнительные ежемесячные прибавки в массе сверх физиологических обычно составляют 200 — 300 г. Поэтому, при дефиците в 1000 г (2 степень) для выведения ребёнка из состояния гипотрофии и достижения долженствующей возрастной массы потребуется 3-5 месяцев, а при гипотрофии 3 степени — не менее 7-9 месяцев. Столь длительный этап реконвалесценции требует от врача жесткого контроля за организацией питания на каждом этапе диетотерапии. При гипотрофии 7 степени, когда толерантность к пище достаточно высокая, расчёт питания проводится на долженствующую массу с полным удовлетворением потребностей ребёнка восновных пищевых ингредиентах, макро — и микронутриентах, витаминах по результатам проведённой коррекции питания. Как исключение, при сниженном аппетите может использоваться период адаптации к пище не более 2-3 дней, когда объём питания снижаем до 2/3 от расчётного, кратность кормлений может быть увеличена на 1 — 2. Для ребёнка с гипотрофией 2 степени объём питания определяется исходя из максимально возможного объёма — 200 мл/кг фактической массы ребёнка, но не более 1 литра. Этот объём принимается за единицу. На этапе разгрузки в зависимости от тяжести состояния и толерантности к пище назначается 1/3,1/2 или 2/3 от расчётного объёма. Недостающий объём пищи компенсируется за счёт питья (рисовый отвар, кипячённая вода, чай, 5% глюкоза, глюкозо-солевые растворы). К концу этапа разгрузки необходимо выйти на 2/3 расчётного объёма питания, который покрывает энергозатраты в основном обмене. В период минимального питания объём пищи увеличивается от 2/3 до 3/4, а иногда и до полного расчётного объёма. Кратность приёма пищи увеличивается на 2-3 кормления. При хорошей толерантности к пище продолжи-тельность этих двух этапов может быть сокращена до 3 — 5 дней. Расчёт пищевых ингредиентов в вышеназванные этапы проводится исходя из следующей потребности: белок — 0,7 — 1,5 — 2,0 г/кг; жиры — 2,0 — 3,0 — 4,0 г/кг; углеводы — 8,0 — 10,0 — 11,0 г/кг; килокалории — 60 — 80 — 100 на кг массы тела. При гипотрофии третьей степени резко нарушаются все виды обмена, состояние ребенка, как правило, бывает крайне тяжелым. Поэтому согласно рекомендациям Национальной программы оптимизации вскармливания детей первого года жизни в Российской Федерации, такие дети нуждаются в проведении интенсивной терапии, использовании энтерального и парентерального питания, что требует стационарного лечения. Гипотрофия третьей степени, вызванная алиментарным фактором, в России встречается в исключительных случаях, т.к. основные нарушения в питании ребенка выявляются рано и необходимая диетическая коррекция рациона этих детей осуществляется еще при первой или второй степени гипотрофии. Причиной гипотрофии третьей степени у детей в нашей стране, как правило, является тяжелая соматическая патология, поэтому своевременная диагностика и лечение причинно-значимого мболевания является основополагающим фактором профилактики и лечения данного состояния. Парентеральное питание начального периода должно проводиться постепенно, с применением исключительно аминокислотных препаратов и растворов глюкозы. Жировые эмульсии при (ипотрофии добавляются в программы парентерального питания юлько спустя 5-7 дней от начала терапии из-за недостаточного их усвоения и высркого риска развития побочных эффектов и осложнений. Парентфальное питание при гипотрофии должно быть сбалансированным и минимальным из-за опасности развития тяжелых метаболических осложнений. Параллельно проводится парентеральная коррекция дегидрагации, нарушений КОС (как правило, ацидоза) и электролитных нарушений. Наиболее оправданным видом энтерального питания при тяжелых формах БЭН является постоянное энтеральное зондовое питание, которое заключается в непрерывном медленном поступлении питательных веществ в ЖКТ (желудок, двенадцатиперстную кишку, тощую кишку) — капельно, оптимально с помощью инфузионного насоса. Медленное введение специализированных продуктов максимально оправдано, так как энергозатраты на переваривание и усвоение питательных веществ в этих условиях гораздо ниже, чем при болюсном введении питательной смеси. При УГОМ улучшается полостное пищеварение и постепенно повышается всасывающая способность кишки. Длительное энтеральное юндовое питание нормализует моторику верхних отделов ЖКТ. Белковый компонент при таком питании модулирует секреторную и кислотообразующую функцию желудка, поддерживает адекватную экзокринную функцию поджелудочной железы и секрецию холецистокинина, обеспечивает нормальную моторику билиарной системы и предотвращает развитие таких осложнений, как билиарный сладж и холелитиаз. Белок, поступающий в тощую кишку, моделирует секрецию хемотрипсина и липазы. Скорость поступления питательной смеси в ЖКТ не должна превышать 3 мл/ мин., калорийная нагрузка — не более 1 ккал/мл, а осмолярность не более 350 млосмол/л. Для энтерального питания у детей раннего возраста с гипотрофией 3 степени в период адаптации к пище должны использоваться специализированные продукты. Наиболее оправданным является применение смесей на основе высоко гидролизованного молочного белка, не содержащих лактозу, обогащенных среднецепочечными триглицеридами («Алфаре», «Нутрилон Пепти ТСЦ», «Нутрилак Пептиди ТСЦ», «Прегистимил»). Они обеспечивают максимальное усвоение питательных веществ в условиях значительного угнетения переваривающей и всасывающей способности пищеварительного канала. Увеличение концентрации вводимой смеси проводят медленно, повышая на 1 % в день (табл.1). Потеря аппетита у ребенка Далее постепенно доводят концентрацию смеси до 13,5 % (физиологической), а при хорошей переносимости — до 15%. Недостающие килокалории, нутриенты и электролиты в период употребления смеси в низкой концентрации компенсируются за счет парентерального питания. Потеря аппетита у ребенка При проведении постоянного энтерального зондового питания должны соблюдаться все правила асептики. Стерильность питательных растворов возможна только при применении готовых жидких питательных смесей. Длительность периода постоянного энтерального зондового питания варьирует от нескольких дней до нескольких недель в зависимости от выраженности нарушенной пищевой толерантности (анорексия, рвота, диарея). Проводится постепенное повышение калорийности и изменение состава пищи, осуществляется постепенный переход на болюсное введение питательной смеси при 7-10 разовом кормлении. При улучшении состояния и аппетита, появлении значимых прибавок массы тела производится полная отмена постоянного зондового кормления. Далее проводится диетотерапия, как у детей с гипотрофией более легкой степени тяжести, основными принципами которой являются омоложение пищи и поэтапность с выделением адаптационного, репарационного (промежуточного) и усиленного этапов питания. На промежуточном этапе диетотерапии ребёнок получает полный объём питания в расчёте на фактическую массу. В дальнейшем постепенно увеличиваем содержание белков и углеводов, а затем жиров, с тем, чтобы к концу этапа выйти на долженствующие возрастные потребности в белках и углеводах, а жиров на среднюю между фактической и долженствующей массой тела. Потребности в пищевых ингредиентах на данном этапе составляют: белок — 3,5 — 4,5 г/кг, углеводов — 13,0 — 14,0 г/кг, жира — 5,0 — 6,0 г/кг, килокалорий — 120 — 130 на кг массы тела. В последние годы отечественные нутрициологи не рекомендуют превышать дозу белка более 3,5 г/кг. К концу этого этапа ребёнок получает полный объём питания, где 2/3 или 1/2 обеспечивает основная смесь, а 1/3 или 1/2-лечебная. Основным показателем адекватности диетотерапии является прибавка массы тела. Хорошей считается прибавка, если она превышает 20 — 30 г/сутки. Возможными причинами плохой прибавки массы являются: неадекватное питание (неправильный расчет питания, ограничение по частоте или объему питания, не соблюдение правил приготовления питательных смесей, отсутствие коррекции питания, недостатки ухода за ребенком), дефицит макро- и микронутриентов, текущий инфекционный процесс, психические проблемы. На этапе оптимального (усиленного) питания диета ребенка соответствует нормальным параметрам за счет расширения ассортимента продуктов, увеличения суточного объема принимаемой пищи, уменьшения числа кормлений. Потребности в пищевых ингредиентах возрастают до максимально допустимых: белок — 3,5 г/кг, жиры — 6,0 — 6,5 г/кг, углеводы — 15 — 1 б г/кг, килокалории — до 135 на кг массы тела и более. При этом энергетическая и белковая нагрузка на фактическую массу тела больше, чем у здоровых детей. Оптимальным результатом диетотерапии в период рекон- валесценции считается достижение долженствующей возрастной месячной прибавки массы тела ребенка и еще 200 — 300 г на покрытие дефицита массы. При проведении диетотерапии наиболее оптимальным продуктом питания является грудное молоко. Однако, как свидетельствует клиническая практика, гипотрофия второй и особенно третьей степени обычно развивается у детей, находящихся на смешанном, а в основном на искусственном вскармливании. В связи с чем питание детей на всех этапах диетотерапии чаще проводится адаптированными молочными смесями. В качестве основных смесей на этапе разгрузки и минимального питания целесообразно применение адаптированных профилактических смесей: Нутрилон Комфорт-1, Нутрилон Комфорт-2. Эти смеси содержат частично гидролизованный белок, который легче переваривается и создает условия для формирования более мягкого стула. Сниженный уровень лактозы облегчает переваривание. Уникальная смесь жиров с бета-пальмитиновой кислотой, повторяющая состав жиров грудного молока, улучшает всасывание жира и кальция. Нутрилон Комфорт содержит смесь пробиотиков, которая активизирует рост нормальной микрофлоры кишечника. Более густая консистенция облегчает продвижение пищи и уменьшает заглатывание воздуха при кормлении. На промежуточном этапе помимо основной смеси необходимо использовать лечебную смесь, которая составляет от 1/3 до 1/2 суточного объёма питания. Сначала лечебная смесь должна обогатить рацион ребёнка белками, при этом содержание жиров должно быть невысоким. Раньше в качестве такой смеси предлагали обезжиренный кефир. Сейчас можно использовать лечебную смесь Хумана ЛЙ+СЦТ, которая является сбалансированным низко жировым и низко лактозным продуктом, обогащенным пищевыми волокнами. В состав этой смеси входит жировой компонент представленный на 50% среднецепочечными триглицеридами, которые хорошо всасываются в пищеварительном тракте без участия желчных кислот и липазы. После адаптации ребёнка к возросшему количеству белка необходимо увеличить в пищевом рационе количество углеводов и жиров, что достигается заменой смеси Хумана Л П+СЦТ на смесь Пре-Нутрилон. Данная смесь содержит нуклеотиды, являющиеся универсальным источником энергии в период активного роста. Содержание триглицеридов со средней длиной цепи способствует лучшему усвоению жирового компонента, а длинноцепочечные жирные кислоты способствуют правильному формированию ЦНС и зрительного анализатора. На этапе оптимального (усиленного) питания следует отказаться от лечебных смесей. Ребёнок в полном объёме должен получать основную смесь, которая может быть профилактической, как на первом этапе диетотерапии, а при нормальной толерантности к пище может быть и базовой: Нутрилон-1,2. В настоящее время разработаны новые смеси диетотерапии для детей с гипотрофией: Ифатрини — до 1 года и Нутрини — для детей от 1 года до б лет. Эти смеси пригодны как для зондового, так и для перорального применения. Основной характеристикой данных смесей является высокое содержание энергии в малом объеме. Вскармливание данными смесями обеспечивает компенсацию дефицита массы и роста, правильное формирование ЦНС и интеллектуального развития, адекватный иммунный ответ, нормальное функционирование ЖКТ. Правильность выбора диеты и пищевой нагрузки должна контролироваться кривой массы тела, характером стула и общим состоянием ребёнка. Выделяюттри типа кривых нарастания массы тела: непрерывный подъём, волнообразная кривая, ступенчатое нарастание массы тела. Непрерывный подъём массы свидетельствует о равновесии процессов усвоения и отложения и хорошем усвоении назначенной пищи. Однако длительный непрерывный подъём массы свидетельствует о напряжении энергии усвоения. С истощением последней непрерывный подъём сменяется малыми нарастаниями или же остановкой в прибавке массы. Это свидетельствует об истощении функциональных возможностей желудочно-кишечного тракта и срыве адаптационных механизмов. Волнообразный тип кривой указывает на способность к накоплению пластического материала при невозможности его прочного фиксирования и свидетельствует об одностороннем стимулировании и напряжённости процессов отложения. Ступенчатое нарастание массы тела является выражением соответствия между процессами усвоения и отложения и свидетельствует о том, что назначенная пища отвечает основным потребностям обмена по количеству и качеству и что организм её усваивает. В конце периода разгрузки после достижения 2/3 объёма пищи широко используется ферментотерапия продолжительностью 3 — 4 недели с проведением в последующем повторных курсов: панзинорм, фестал, мексаза, мезим-форте и др. При высоком содержании в копрограмме больных нейтрального жира и жирных кислот показаны панкреатин, панцитрат, креон. Витаминотерапия при лечении больных с гипотрофией используется с заместительной и стимулирующей целями. В первые дни витамины (аскорбиновая кислота, В1, В6) вводятся парентерально, а в дальнейшем даются внутрь. С этапа минимального питания проводятся чередующиеся курсы витаминотерапии: тиамин (ВТ) по 10 — 15 мг в сутки оказывает стимулирующее действие на желудочно-кишечную секрецию, рибофлавин (В2) по б — Т 0 мг для стимуляции обменных процессов, пиридоксин (В6) 2,5% и 5% раствор по 0,5 мл через день усиливает синтез аминокислот, витамин В12 по 30-50 мкг усиливает эритропоэз, никотиновая кислота (РР) по 10 — 20 мг в сутки. С целью улучшения обменных процессов истимуляции эндогенной продукции кортикостероидов показано назначение пантотеновой (В5) и пангамовой (В15) кислот по 0,05 три раза в сутки. Назначение жирорастворимых витаминов возможно при достаточном обеспечении количества жира в дневном рационе. С целью коррекции дисбиотических нарушений кишечника на втором и третьем этапах диетотерапии адаптированными смесями с про- и пребиотиками показано назначение биологически активных препаратов: бифидум-бактерин (первое полугодие), бификол и колибактерин (второе полугодие) по 2 — 5 доз 3-4 раза в сутки, лактобактерин, линекс и др. В последнее время появились препараты синбиоти, включающие в себя пре- и пробиотики. Детям с б месяцев рекомендуется препарат Нормобакт, в состав которого входят 4 миллиарда живых бактерий и пребиотик рафтилоза, получаемый из цикория. Детям раннего возраста достаточно 1 саше в день в течение 10 дней. Стимулирующая терапия проводится тогда, когда обеспечено достаточное количество питания и ребёнок начал прибавлять в массе. Она заключается в назначении чередующихся курсов лечения: апилак (0,005 — 0,01) и метацил (5 мг) в свечах, настойки элеутерококка, женьшеня (1-3 капли) три раза в день и др. При гипотрофии третьей степени в конце этапа промежуточного питания, т.е. в период стабилизации белкового обмена, возможно проведение гормональной терапии: инсулинотерапия — по 2 — 4 ед. с глюкозой (1 ед. инсулина на 4 г глюкозы), нерабол по 0,1 мг/кг в сутки или ретаболил по 1 мг/кг 1 раз в две — три недели в течение одного, двух месяцев. В дальнейшем, особенно при токсико-септических состояниях, под контролем иммунограммы показана иммунокоррегирующая терапия. Симптоматическая терапия зависит от клинической картины гипотрофии и сопутствующих состояний. При наличии анемии, рахита в период стабилизации толерантности к пище целесообразно использование препаратов железа, водорастворимого витамина ДЗ в лечебных дозах. Терапия симптоматических или вторичных гипотрофий должна быть направлена на лечение основного заболевания. Профилактика Предупреждение гипотрофии зависит от своевременности устранения факторов, предрасполагающих к её развитию. Поэтому профилактику гипотрофии целесообразно подразделить на антенатальную и постнатальную. При антенатальной профилактике основное внимание должно уделяться устранению или ослаблению воздействия на плод преплацентарных причин. При постнатальной гипотрофии необходимо исключить воздействие экзогенных факторов и прежде всего пропаганда естественного вскармливания, своевременная диагностика гипогалактии у матери, коррекция питания при смешанном и искусственном вскармливании, соблюдение режима ухода и воспитания ребёнка, предупреждение и лечение различных инфекционных заболеваний, систематический контроль за физическим развитием. При наличии эндогенных причин необходима своевременная диагностика и лечение основного заболевания. Потеря аппетита у ребенка…
|

 Неинфекционные диареи у детей раннего возраста. Хронические расстройства питания. Крас. ГМА, кафедра детских болезней № 2, доцент Прокопцева Н. Л.
Неинфекционные диареи у детей раннего возраста. Хронические расстройства питания. Крас. ГМА, кафедра детских болезней № 2, доцент Прокопцева Н. Л.  Цели и задачи: Изложить современные представления p об этиопатогенезе неинфекционных диарей у детей раннего возраста, общую семиотику, особенности клинических проявлений в зависимости от характера питания и нарушений процесса пищеварения, особенностях вскармливания и лечения при различных видах диарей; p о видах хронических расстройств питания, их причинах, клинике, методах коррекции.
Цели и задачи: Изложить современные представления p об этиопатогенезе неинфекционных диарей у детей раннего возраста, общую семиотику, особенности клинических проявлений в зависимости от характера питания и нарушений процесса пищеварения, особенностях вскармливания и лечения при различных видах диарей; p о видах хронических расстройств питания, их причинах, клинике, методах коррекции.  План лекции p Морфологические и функциональные особенности пищеварительного тракта у детей раннего возраста. p Варианты диарей, в зависимости от характера питания и нарушений процесса пищеварения. p Клиника простой диспепсии. p Синдром мальабсорбции (лактазная недостаточность, целиакия, муковисцидоз, эксудативная энтеропатия. p Лечение неинфекционной диспепсии. p Варианты дистрофий p Гипотрофия, этиология, патогенез, клиника, лечение. p Паратрофия, причины, клиника, диетотерапия. p Понятие о гипостатуре.
План лекции p Морфологические и функциональные особенности пищеварительного тракта у детей раннего возраста. p Варианты диарей, в зависимости от характера питания и нарушений процесса пищеварения. p Клиника простой диспепсии. p Синдром мальабсорбции (лактазная недостаточность, целиакия, муковисцидоз, эксудативная энтеропатия. p Лечение неинфекционной диспепсии. p Варианты дистрофий p Гипотрофия, этиология, патогенез, клиника, лечение. p Паратрофия, причины, клиника, диетотерапия. p Понятие о гипостатуре.  ДИАРЕЯ (понос) – Учащенное и обильное опорожнение кишечника, обычно жидкими фекальными массами в результате нарушения всасывания воды и электролитов в кишечнике. Особенности стула при поносе: p учащение может быть незначительным (на 2 -3 дефекации больше, чем в норме, и трудно сосчитываемым), p количество каловых масс превышает 10 г/кг/сут. , p стул при поносе бывает различной консистенции – от кашецеобразного до водянистого, жидкого (в зависимости от степени содержания воды).
ДИАРЕЯ (понос) – Учащенное и обильное опорожнение кишечника, обычно жидкими фекальными массами в результате нарушения всасывания воды и электролитов в кишечнике. Особенности стула при поносе: p учащение может быть незначительным (на 2 -3 дефекации больше, чем в норме, и трудно сосчитываемым), p количество каловых масс превышает 10 г/кг/сут. , p стул при поносе бывает различной консистенции – от кашецеобразного до водянистого, жидкого (в зависимости от степени содержания воды).  Анатомо-физиологические особенности ЖКТ ребенка, предрасполагающие к высокой заболеваемости диареей: n снижение слизеобразующей функции кишечника, n высокий р. Н желудочного сока, n снижение содержания секреторного Ig. А, n низкий запас транспортных систем, регулирующих реабсорбцию натрия, хлора и других электролитов, n низкая барьерная функция кишечника, n пониженная дезинтоксикационная функция печени.
Анатомо-физиологические особенности ЖКТ ребенка, предрасполагающие к высокой заболеваемости диареей: n снижение слизеобразующей функции кишечника, n высокий р. Н желудочного сока, n снижение содержания секреторного Ig. А, n низкий запас транспортных систем, регулирующих реабсорбцию натрия, хлора и других электролитов, n низкая барьерная функция кишечника, n пониженная дезинтоксикационная функция печени.  Окончательное становление ЖКТ заканчивается к 10 -12 годам. Ранний перевод на искусственное вскармливание, грубое нарушение нутритивных правил не только изменяет нормальный онтогенетический алгоритм пищеварительной системы, но и лежит в основе разнообразных расстройств пищеварения.
Окончательное становление ЖКТ заканчивается к 10 -12 годам. Ранний перевод на искусственное вскармливание, грубое нарушение нутритивных правил не только изменяет нормальный онтогенетический алгоритм пищеварительной системы, но и лежит в основе разнообразных расстройств пищеварения.  Заболевания, сопровождающиеся поносом у грудных детей p болезни мальабсорбции (целиакия, ферментопатии ЖКТ, муковисцидоз и др. ), p гастроэнтериты вирусной, бактериальной или грибковой этиологии, p алиментарные расстройства.
Заболевания, сопровождающиеся поносом у грудных детей p болезни мальабсорбции (целиакия, ферментопатии ЖКТ, муковисцидоз и др. ), p гастроэнтериты вирусной, бактериальной или грибковой этиологии, p алиментарные расстройства.  Диспепсия – острое расстройство пищеварения алиментарного (неинфекционного) происхождения у детей грудного возраста, характеризующееся рвотой, поносом без значительного нарушения общего состояния. dys- — нарушение + pepsis — варение, переваривание
Диспепсия – острое расстройство пищеварения алиментарного (неинфекционного) происхождения у детей грудного возраста, характеризующееся рвотой, поносом без значительного нарушения общего состояния. dys- — нарушение + pepsis — варение, переваривание  Патогенез диспепсии Неправильный перевод на другой тип вскармливания, количественный и/или качественный перекорм, приготовление пищи из несовместимых продуктов, введении в рацион продуктов, не соответствующих возрасту Не достаточная обработка пищи на уровне желудка и начального отдела тонкой кишки Поступление неподготовленного химуса с избыточным содержанием нерасщепленных белков, углеводов и жиров в дистальные отделы тонкой кишки Расстройства пищеварения
Патогенез диспепсии Неправильный перевод на другой тип вскармливания, количественный и/или качественный перекорм, приготовление пищи из несовместимых продуктов, введении в рацион продуктов, не соответствующих возрасту Не достаточная обработка пищи на уровне желудка и начального отдела тонкой кишки Поступление неподготовленного химуса с избыточным содержанием нерасщепленных белков, углеводов и жиров в дистальные отделы тонкой кишки Расстройства пищеварения 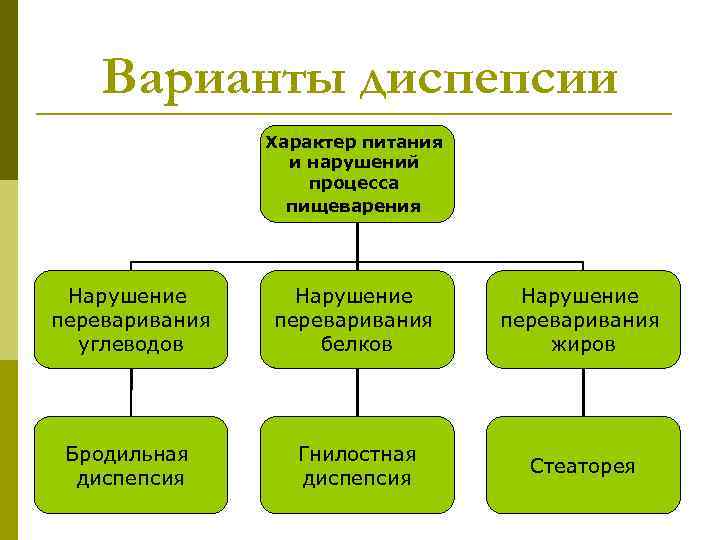 Варианты диспепсии Характер питания и нарушений процесса пищеварения Нарушение переваривания углеводов белков жиров Бродильная Гнилостная Стеаторея диспепсия
Варианты диспепсии Характер питания и нарушений процесса пищеварения Нарушение переваривания углеводов белков жиров Бродильная Гнилостная Стеаторея диспепсия  Бродильная диспепсия p Возникает в случае избыточного поступления углеводов в составе пищевого химуса в дистальные отделы кишки. p Развивается при чрезмерном перекармливания ребенка грудным молоком, искусственными смесями, прикормами с высоким содержанием углеводов (фруктовые и овощные пюре). p Нерасщепленные сахара оказывают осмотическое влияние, привлекая в просвет кишки воду, а также в результате бактериального брожения сахаролитической флорой превращаются в жирные кислоты (молочную, уксусную). В результате — усиление перистальтики и бродильные поносы. p Стул жидкий, пенистый, с отчетливым кислым запахом. p Преобладают лактобактерии, бифидум-флора.
Бродильная диспепсия p Возникает в случае избыточного поступления углеводов в составе пищевого химуса в дистальные отделы кишки. p Развивается при чрезмерном перекармливания ребенка грудным молоком, искусственными смесями, прикормами с высоким содержанием углеводов (фруктовые и овощные пюре). p Нерасщепленные сахара оказывают осмотическое влияние, привлекая в просвет кишки воду, а также в результате бактериального брожения сахаролитической флорой превращаются в жирные кислоты (молочную, уксусную). В результате — усиление перистальтики и бродильные поносы. p Стул жидкий, пенистый, с отчетливым кислым запахом. p Преобладают лактобактерии, бифидум-флора.  Гнилостная диспепсия p Является следствием нарушения переваривания белков. p Чрезмерное количество белковых продуктов попадает в нижние отделы кишечника, где под влиянием различных бактерий начинаются гнилостные процессы. p Бактериальное расщепление белков путем гниения в кишечнике содействует образованию токсичных продуктов обмена (индол, скатол, уксусная кислота) и газов. p Раздражение рецепторов слизистой оболочки токсическими продуктами ведет к появлению защитной реакции в виде усиления перистальтики кишечника и появлению рвоты и поноса. p Стул с большим содержанием слизи, зловонный. p Преобладают коли-бактерии, энтерококки, стафилококки и некоторые другие условно-патогенные микроорганизмы.
Гнилостная диспепсия p Является следствием нарушения переваривания белков. p Чрезмерное количество белковых продуктов попадает в нижние отделы кишечника, где под влиянием различных бактерий начинаются гнилостные процессы. p Бактериальное расщепление белков путем гниения в кишечнике содействует образованию токсичных продуктов обмена (индол, скатол, уксусная кислота) и газов. p Раздражение рецепторов слизистой оболочки токсическими продуктами ведет к появлению защитной реакции в виде усиления перистальтики кишечника и появлению рвоты и поноса. p Стул с большим содержанием слизи, зловонный. p Преобладают коли-бактерии, энтерококки, стафилококки и некоторые другие условно-патогенные микроорганизмы.  Стеаторея p Появляется при чрезмерном содержании жиров в пище. p В результате неправильного расщепления жира в кишечнике образуются жирные кислоты, которые, нейтрализуются путем поступления из межклеточной жидкости и тканей организма солей кальция, магния, натрия, калия. Эти соли вступают в реакцию с жирными кислотами и образуют мыла жирных кислот. p Стул обильный, блестящий с комочками, плохо смывается с пеленки или горшка.
Стеаторея p Появляется при чрезмерном содержании жиров в пище. p В результате неправильного расщепления жира в кишечнике образуются жирные кислоты, которые, нейтрализуются путем поступления из межклеточной жидкости и тканей организма солей кальция, магния, натрия, калия. Эти соли вступают в реакцию с жирными кислотами и образуют мыла жирных кислот. p Стул обильный, блестящий с комочками, плохо смывается с пеленки или горшка.  Клиника диспепсии p Предвестники кишечных расстройств: общее беспокойство, частый плач, снижение аппетита или отказ от еды, нарушение сна. p Температура тела нормальная или субфебрильная. p На высоте диспепсии – одно-/двукратная рвота. p Главный симптом – расстройство стула (характер стула зависит от особенностей вскармливания ). p Периодически – приступы абдоминальной боли ( «кишечная колика» ) из-за растяжения кишечной стенки скопившимися газами, после отхождения которых ребенок успокаивается.
Клиника диспепсии p Предвестники кишечных расстройств: общее беспокойство, частый плач, снижение аппетита или отказ от еды, нарушение сна. p Температура тела нормальная или субфебрильная. p На высоте диспепсии – одно-/двукратная рвота. p Главный симптом – расстройство стула (характер стула зависит от особенностей вскармливания ). p Периодически – приступы абдоминальной боли ( «кишечная колика» ) из-за растяжения кишечной стенки скопившимися газами, после отхождения которых ребенок успокаивается.  Клинические симптомы, выявляемые при осмотре ребенка с диспепсией p Состояние ребенка относительно удовлетворительное. p В момент приступа болей младенец беспокоен, громко плачет, не склонен к проведению осмотра. p Визуально выявляется легкая бледность и сухость кожных покровов. p Полость рта обычной окраски, слизистые немного суховатые (блестящие), язык обложен белым налетом. p Живот вздут, на высоте колики — напряжен, при пальпации урчание и чувство «переливания жидкости» . p Анус сомкнут, чаще всего наблюдается незначительная гиперемия перианальной области и опрелости в области ягодиц вследствие раздражения кожи.
Клинические симптомы, выявляемые при осмотре ребенка с диспепсией p Состояние ребенка относительно удовлетворительное. p В момент приступа болей младенец беспокоен, громко плачет, не склонен к проведению осмотра. p Визуально выявляется легкая бледность и сухость кожных покровов. p Полость рта обычной окраски, слизистые немного суховатые (блестящие), язык обложен белым налетом. p Живот вздут, на высоте колики — напряжен, при пальпации урчание и чувство «переливания жидкости» . p Анус сомкнут, чаще всего наблюдается незначительная гиперемия перианальной области и опрелости в области ягодиц вследствие раздражения кожи.  Дифференциальный диагноз простой диспепсии Прежде всего надо исключить: p Заболевания, требующие безотлагательной хирургической помощи (инвагинация, дивертикулит Меккеля и др. ). p Стертые формы дизентерии, колиэнтерита, сальманеллеза и других кишечных инфекций (при наличие повышенной температуры, отсутствии быстрого эффекта от правильно проводимой терапии, наличии признаков токсикоза). В случае госпитализации ребенка необходимо произвести тщательный бактериологический анализ кала, при нахождении заболевшего в доме ребенка или детском саду его надо изолировать, кал отправить на бактериологическое исследование.
Дифференциальный диагноз простой диспепсии Прежде всего надо исключить: p Заболевания, требующие безотлагательной хирургической помощи (инвагинация, дивертикулит Меккеля и др. ). p Стертые формы дизентерии, колиэнтерита, сальманеллеза и других кишечных инфекций (при наличие повышенной температуры, отсутствии быстрого эффекта от правильно проводимой терапии, наличии признаков токсикоза). В случае госпитализации ребенка необходимо произвести тщательный бактериологический анализ кала, при нахождении заболевшего в доме ребенка или детском саду его надо изолировать, кал отправить на бактериологическое исследование.  Лабораторные изменения при неинфекционных диспепсиях p В кале определяется большое количество нейтрального жира, свободных жирных кислот, слизь, лейкоциты единичные. p Посевы кала на патогенную флору отрицательные. p При анализе крови определяется ацидоз, несколько понижается уровень калия, кальция, натрия и хлоридов крови. p В моче, приобретающей резкий запах, увеличивается количество аммиака (сдвиг в сторону ацидоза). p Высокая относительная плотность мочи свидетельствует о ранней стадии дегидратации.
Лабораторные изменения при неинфекционных диспепсиях p В кале определяется большое количество нейтрального жира, свободных жирных кислот, слизь, лейкоциты единичные. p Посевы кала на патогенную флору отрицательные. p При анализе крови определяется ацидоз, несколько понижается уровень калия, кальция, натрия и хлоридов крови. p В моче, приобретающей резкий запах, увеличивается количество аммиака (сдвиг в сторону ацидоза). p Высокая относительная плотность мочи свидетельствует о ранней стадии дегидратации.  Синдром мальабсорбции – дефект всасывания в кишечнике У детей раннего возраста встречается при: p непереносимости лактозы (реже других углеводов) и p непереносимости белков коровьего молока, p целиакии (непереносимости глютена). p при заболеваниях наследственного характера (муковисцидоз, врожденная хлоридная диарея, энтеропатический акродерматит, а-β- липопротеинемия, врожденный дефицит липазы, трипсина, энтерокиназы, врожденные иммунодефицитные состояния и пр. ).
Синдром мальабсорбции – дефект всасывания в кишечнике У детей раннего возраста встречается при: p непереносимости лактозы (реже других углеводов) и p непереносимости белков коровьего молока, p целиакии (непереносимости глютена). p при заболеваниях наследственного характера (муковисцидоз, врожденная хлоридная диарея, энтеропатический акродерматит, а-β- липопротеинемия, врожденный дефицит липазы, трипсина, энтерокиназы, врожденные иммунодефицитные состояния и пр. ).  Лактазная недостаточность Проявляется бродильной диареей. У больного ребенка наблюдаются: p частый (8 -10 раз в сутки и более) жидкий пенистый стул с большим водяным пятном и кислым запахом; p вздутие живота, урчание, боли в животе; p наличие углеводов в фекалиях (более 2 г%); p кислая реакция стула (р. Н менее 5, 5); p возможное развитие обезвоживания; p относительно редкое развитие тяжелой гипотрофии.
Лактазная недостаточность Проявляется бродильной диареей. У больного ребенка наблюдаются: p частый (8 -10 раз в сутки и более) жидкий пенистый стул с большим водяным пятном и кислым запахом; p вздутие живота, урчание, боли в животе; p наличие углеводов в фекалиях (более 2 г%); p кислая реакция стула (р. Н менее 5, 5); p возможное развитие обезвоживания; p относительно редкое развитие тяжелой гипотрофии.  Методы оценки лактазной активности слизистой оболочки кишечника: p Лактозотолерантный тест: определение прироста гликемии в течение 1 -2 часов после пероральной нагрузки лактозой в дозе 1 -2 г/кг веса ребенка (но не более 50 г). Тест считается (+) приросте гликемии менее, чем на 20% от исходного уровня, а также при развитии диспептических расстройств в течение суток после нагрузки. p Определение активности лактазы в биоптате слизистой оболочки тонкой кишки.
Методы оценки лактазной активности слизистой оболочки кишечника: p Лактозотолерантный тест: определение прироста гликемии в течение 1 -2 часов после пероральной нагрузки лактозой в дозе 1 -2 г/кг веса ребенка (но не более 50 г). Тест считается (+) приросте гликемии менее, чем на 20% от исходного уровня, а также при развитии диспептических расстройств в течение суток после нагрузки. p Определение активности лактазы в биоптате слизистой оболочки тонкой кишки.  Непереносимость белков коровьего молока (аллергическая энтеропатия) Наиболее типичные синдромы: p белок-теряющая энтеропатия (длительная диарея с обнаружением плазменных белков в кале, дистрофия, безбелковые отеки); p железодефицитная анемия, связанная с хронической продолжительной потерей крови через кишечник (положительная реакция на скрытую кровь в кале); p классический энтероколит.
Непереносимость белков коровьего молока (аллергическая энтеропатия) Наиболее типичные синдромы: p белок-теряющая энтеропатия (длительная диарея с обнаружением плазменных белков в кале, дистрофия, безбелковые отеки); p железодефицитная анемия, связанная с хронической продолжительной потерей крови через кишечник (положительная реакция на скрытую кровь в кале); p классический энтероколит.  Методы диагностики аллергической энтеропатии: p иммунологический: кожные тесты и определение специфических Ig. Е-антител к пищевым аллергенам; p морфологический: изменения кишечных ворсинок при эндоскопическом исследовании ЖКТ и гистологическом исследовании биоптата слизистой оболочки тонкой кишки; p диетологический: исчезновение симптомов заболевания при исключении подозреваемого протеина из диеты и их возобновление при проведении пищевой нагрузки.
Методы диагностики аллергической энтеропатии: p иммунологический: кожные тесты и определение специфических Ig. Е-антител к пищевым аллергенам; p морфологический: изменения кишечных ворсинок при эндоскопическом исследовании ЖКТ и гистологическом исследовании биоптата слизистой оболочки тонкой кишки; p диетологический: исчезновение симптомов заболевания при исключении подозреваемого протеина из диеты и их возобновление при проведении пищевой нагрузки.  Целиакия (глютеновая энтеропатия) Проявляется атрофическими изменениями слизистой оболочки тонкой кишки под влиянием глютена – белка, содержащегося в пшенице, ржи, ячмене, овсе. Клинические проявления при введении прикорма с включением глютен-содержащих продуктов : p обильный, зловонный, кашецеобразный или жидкий стул, p нередко повторная рвота, p ухудшение аппетита, p изменение поведения (ребенок становится вялым, безразличным к окружающему или негативным, раздражительным), p выраженное похудание, вплоть до кахексии, p атрофия проксимальных групп мышц при увеличении живота (вид «паука» ), p гипопротеимнемические отеки, электролитные нарушения, гипокальциемические судороги, остеопороз, p анемия, авитаминоз, p отсутствие эффекта от применения ферментных, железосодержащих, антибактериальных и биопрепаратов, инфузионной терапии, p нормализация состояния при исключении из пищи глютена, рецидив после вновь введенного в пищу глютена Решающее диагностическое значение придают определению антиаглиадиновых антител и антител к эндонизию, а также биопсии слизистой оболочки верхнего отдела тонкой кишки.
Целиакия (глютеновая энтеропатия) Проявляется атрофическими изменениями слизистой оболочки тонкой кишки под влиянием глютена – белка, содержащегося в пшенице, ржи, ячмене, овсе. Клинические проявления при введении прикорма с включением глютен-содержащих продуктов : p обильный, зловонный, кашецеобразный или жидкий стул, p нередко повторная рвота, p ухудшение аппетита, p изменение поведения (ребенок становится вялым, безразличным к окружающему или негативным, раздражительным), p выраженное похудание, вплоть до кахексии, p атрофия проксимальных групп мышц при увеличении живота (вид «паука» ), p гипопротеимнемические отеки, электролитные нарушения, гипокальциемические судороги, остеопороз, p анемия, авитаминоз, p отсутствие эффекта от применения ферментных, железосодержащих, антибактериальных и биопрепаратов, инфузионной терапии, p нормализация состояния при исключении из пищи глютена, рецидив после вновь введенного в пищу глютена Решающее диагностическое значение придают определению антиаглиадиновых антител и антител к эндонизию, а также биопсии слизистой оболочки верхнего отдела тонкой кишки.  Лечение диарей При выявлении у ребенка диареи (даже при отсутствии клинических признаков обезвоживания) необходимо сразу же приступить к нормализации вводно- электролитного баланса.
Лечение диарей При выявлении у ребенка диареи (даже при отсутствии клинических признаков обезвоживания) необходимо сразу же приступить к нормализации вводно- электролитного баланса.  Путь введения жидкости? p При нетяжелом общем состоянии, легкой степени дегидратации (потери до 5% от массы тела), с сохранением сознания и отсутствием рвоты нужно стараться проводить регидратацию наиболее физиологичным путем, т. е. «per os» . p При токсикозе с эксикозом 2 -3 степени и частой рвоте оральная регидратация дополняется парентеральной.
Путь введения жидкости? p При нетяжелом общем состоянии, легкой степени дегидратации (потери до 5% от массы тела), с сохранением сознания и отсутствием рвоты нужно стараться проводить регидратацию наиболее физиологичным путем, т. е. «per os» . p При токсикозе с эксикозом 2 -3 степени и частой рвоте оральная регидратация дополняется парентеральной.  Что вводить? p Для пероральной регидратации используют растворы солей – оралит, регидрон, цитроглюкосолан (они составляют ½-2/3 общего суточного объема, необходимого ребенку), питьевую воду, чай, отвар шиповника. p При внутривенном введении жидкости определение стартового состава инфузионной смеси зависит от вида дегидратации: Ø При признаках гипертонической дегидратации (таких как раздражительность, гипертония мышц, жажда, нормальный диурез, повышение температуры тела и т. д. ) – смесь 5% раствора глюкозы и 0, 9% раствора Na. Cl в соотношении 3: 1, Ø При частой рвоте и признаках гипотонической дегидратации (выраженная вялость, мышечная и артериальная гипотония, снижение температуры тела, брадипноэ, олигоанурия) – те же растворы, но в равном соотношении (1: 1),
Что вводить? p Для пероральной регидратации используют растворы солей – оралит, регидрон, цитроглюкосолан (они составляют ½-2/3 общего суточного объема, необходимого ребенку), питьевую воду, чай, отвар шиповника. p При внутривенном введении жидкости определение стартового состава инфузионной смеси зависит от вида дегидратации: Ø При признаках гипертонической дегидратации (таких как раздражительность, гипертония мышц, жажда, нормальный диурез, повышение температуры тела и т. д. ) – смесь 5% раствора глюкозы и 0, 9% раствора Na. Cl в соотношении 3: 1, Ø При частой рвоте и признаках гипотонической дегидратации (выраженная вялость, мышечная и артериальная гипотония, снижение температуры тела, брадипноэ, олигоанурия) – те же растворы, но в равном соотношении (1: 1),  Коррекция содержания калия Калий надо вводить из расчета 2, 5 -3 ммоль/кг/сут (1 мл 7, 5 KCL содержит 1 ммоль калия), в тяжелых случаях – 4 -4, 5 ммоль/кг/сут. Более точный расчет ведется по формуле: количество ммоль К = 0, 5 х (концентрация К в норме – концентрация К у больного) х масса тела в кг. Общая суточная доза делится на 3 -5 приемов и вводится равномерно в течение суток. Вводить калий надо капельно в достаточном количестве инфузионной жидкости, так чтобы его концентрация в инфузате не превышала 1%.
Коррекция содержания калия Калий надо вводить из расчета 2, 5 -3 ммоль/кг/сут (1 мл 7, 5 KCL содержит 1 ммоль калия), в тяжелых случаях – 4 -4, 5 ммоль/кг/сут. Более точный расчет ведется по формуле: количество ммоль К = 0, 5 х (концентрация К в норме – концентрация К у больного) х масса тела в кг. Общая суточная доза делится на 3 -5 приемов и вводится равномерно в течение суток. Вводить калий надо капельно в достаточном количестве инфузионной жидкости, так чтобы его концентрация в инфузате не превышала 1%.  Коррекция ацидоза Для борьбы с ацидозом применяют раствор бикарбоната натрия. Расчет ведется по формуле: количество ммоль Na. HCO 3 = 0, 3 х ВЕ х масса тела в кг 1 мл 8, 4% раствора Na. HCO 3 содержит 1 ммоль бикарбоната. Растворы Na. HCO 3 необходимо вводить дробно, в 3 -4 приема, капельно и только в общем составе инфузионной жидкости, под контролем КОС.
Коррекция ацидоза Для борьбы с ацидозом применяют раствор бикарбоната натрия. Расчет ведется по формуле: количество ммоль Na. HCO 3 = 0, 3 х ВЕ х масса тела в кг 1 мл 8, 4% раствора Na. HCO 3 содержит 1 ммоль бикарбоната. Растворы Na. HCO 3 необходимо вводить дробно, в 3 -4 приема, капельно и только в общем составе инфузионной жидкости, под контролем КОС.  Объем вводимой жидкости? Оральная регидратация проводится в 2 этапа: Ø в первые 4 -6 часов ребенок должен получить объем жидкости, равный дефициту массы тела за счет обезвоживания: количество жидкости = % потери массы тела · 10 · масса тела в кг. Ø в последующие 18 часов: количество жидкости = объем физиологической потребности + объем патологических потерь с рвотой и стулом. При водянистых диареях теряется с жидким стулом и рвотой 10 мл жидкости на 1 кг массы тела на каждое испражнение. При гипертермии добавляют по 10 мл инфузата на каждый градус температуры тела, превышающей 37˚.
Объем вводимой жидкости? Оральная регидратация проводится в 2 этапа: Ø в первые 4 -6 часов ребенок должен получить объем жидкости, равный дефициту массы тела за счет обезвоживания: количество жидкости = % потери массы тела · 10 · масса тела в кг. Ø в последующие 18 часов: количество жидкости = объем физиологической потребности + объем патологических потерь с рвотой и стулом. При водянистых диареях теряется с жидким стулом и рвотой 10 мл жидкости на 1 кг массы тела на каждое испражнение. При гипертермии добавляют по 10 мл инфузата на каждый градус температуры тела, превышающей 37˚.  Объем вводимой жидкости? Объем инфузионной регидрационной терапии рассчитывается по формуле: V = (N + D + P) – (Oм + Оп), где V – общий объем жидкости в сутки, N – нормальные суточные потребности в жидкости, D – дефицит массы тела, P – продолжающиеся потери, Oм – объем молока, Оп – объем питьевых растворов. Продолжают внутривенную инфузионную терапию до улучшения самочувствия ребенка, прекращения рвоты, появления возможности оральной регидратации.
Объем вводимой жидкости? Объем инфузионной регидрационной терапии рассчитывается по формуле: V = (N + D + P) – (Oм + Оп), где V – общий объем жидкости в сутки, N – нормальные суточные потребности в жидкости, D – дефицит массы тела, P – продолжающиеся потери, Oм – объем молока, Оп – объем питьевых растворов. Продолжают внутривенную инфузионную терапию до улучшения самочувствия ребенка, прекращения рвоты, появления возможности оральной регидратации.  Коррекция вскармливания (диетотерапия) p Необходимо проанализировать и исправить алиментарные ошибки. p Разгрузка в питании (до 30 -50% от физиологической потребности) и дробное дозированное питание. Недостающий объем питания обязательно восполняется жидкостью. p При естественном вскармливании обычно в первый день сокращают время прикладывания к груди до 3 -4 минут (обычно за одну минуту ребенок высасывает 20 мл). p При смешанном вскармливании следует ограничиться только кормлением грудью на ограниченное время (без докорма смесями). p При искусственном вскармливании вместо обычной пищи на 1 — 2 кормления ребенка переводят на водно-чайную диету. Во время водно- чайной диеты используют солевые растворы — регидрон, оралит, физиологический раствор, 2 -5 % раствор глюкозы, зеленый чай (освобожденный от чаинок) и др. Далее ребенку дают адаптированные кисломолочные смеси в половинном возрастном объеме. p С каждым днем количество пищи увеличивается, примерно к 5 -6 дню объем питания должен достигать объема, который ребенок употреблял до заболевания. p Со второй недели от начала заболевания можно вводить прикорм, если ребенок получал его до болезни, но вводить следует постепенно, соблюдая все требования по введению нового продукта питания. p Соки назначают осторожно, особенно при бродильной диспепсии, не ранее второй — третьей недели от начала заболевания.
Коррекция вскармливания (диетотерапия) p Необходимо проанализировать и исправить алиментарные ошибки. p Разгрузка в питании (до 30 -50% от физиологической потребности) и дробное дозированное питание. Недостающий объем питания обязательно восполняется жидкостью. p При естественном вскармливании обычно в первый день сокращают время прикладывания к груди до 3 -4 минут (обычно за одну минуту ребенок высасывает 20 мл). p При смешанном вскармливании следует ограничиться только кормлением грудью на ограниченное время (без докорма смесями). p При искусственном вскармливании вместо обычной пищи на 1 — 2 кормления ребенка переводят на водно-чайную диету. Во время водно- чайной диеты используют солевые растворы — регидрон, оралит, физиологический раствор, 2 -5 % раствор глюкозы, зеленый чай (освобожденный от чаинок) и др. Далее ребенку дают адаптированные кисломолочные смеси в половинном возрастном объеме. p С каждым днем количество пищи увеличивается, примерно к 5 -6 дню объем питания должен достигать объема, который ребенок употреблял до заболевания. p Со второй недели от начала заболевания можно вводить прикорм, если ребенок получал его до болезни, но вводить следует постепенно, соблюдая все требования по введению нового продукта питания. p Соки назначают осторожно, особенно при бродильной диспепсии, не ранее второй — третьей недели от начала заболевания.  Питание детей с лактазной недостаточностью p В случае искусственного вскармливания используются: Ø безлактозные и низколактозные адаптированные смеси на основе коровьего молока (Нан безлактозный, Нутрилон низколактозный, Нутрилак низколактозный, Мамекс безлактозный, Прегестемил, Портаген) Ø адаптированные смеси на основе изолята соевого белка (Нутрилон Соя, Фрисосой, Энфамил Соя, Хумана–СЛ). p В рационе детей, находящихся на естественном вскармливании оказывается возможным сохранение женского молока в количестве ½-1/3 от объема каждого кормления. Недостающий объем восполняют безлактозными адаптированными смесями. p Можно использовать препарат «Лактразу» немецкой фирмы Schwarz Farma, содержащий лактазу, добавляя его по 1 -2 капсулы на 1 литр женского молока или адаптированной молочной смеси.
Питание детей с лактазной недостаточностью p В случае искусственного вскармливания используются: Ø безлактозные и низколактозные адаптированные смеси на основе коровьего молока (Нан безлактозный, Нутрилон низколактозный, Нутрилак низколактозный, Мамекс безлактозный, Прегестемил, Портаген) Ø адаптированные смеси на основе изолята соевого белка (Нутрилон Соя, Фрисосой, Энфамил Соя, Хумана–СЛ). p В рационе детей, находящихся на естественном вскармливании оказывается возможным сохранение женского молока в количестве ½-1/3 от объема каждого кормления. Недостающий объем восполняют безлактозными адаптированными смесями. p Можно использовать препарат «Лактразу» немецкой фирмы Schwarz Farma, содержащий лактазу, добавляя его по 1 -2 капсулы на 1 литр женского молока или адаптированной молочной смеси.  Искусственное вскармливании детей с непереносимостью белков коровьего молока p Специализированные смеси на основе изолята соевого белка и безмолочные продукты прикорма. p При непереносимости соевых смесей используют лечебные смеси на основе глубокого гидролизата белка (Нутрилон Пепти ТСЦ, Альфаре, Прегестимил, Нутрамиген, Алиментум).
Искусственное вскармливании детей с непереносимостью белков коровьего молока p Специализированные смеси на основе изолята соевого белка и безмолочные продукты прикорма. p При непереносимости соевых смесей используют лечебные смеси на основе глубокого гидролизата белка (Нутрилон Пепти ТСЦ, Альфаре, Прегестимил, Нутрамиген, Алиментум).  Вскармливание детей, больных целиакией из рациона исключаются глютен- содержащие продукты на основе: p пшеничной, p ржаной, p овсяной, p ячменной муки.
Вскармливание детей, больных целиакией из рациона исключаются глютен- содержащие продукты на основе: p пшеничной, p ржаной, p овсяной, p ячменной муки.  Медикаментозная терапия p Ферментотерапия: микрокапсулированный препарат панкреатина — креон (по 1 капсуле 3 — 4 раза в сутки во время еды, содержимое капсулы смешивается с небольшим количеством пищи). p Энтеросорбенты: смекта (до 1 года жизни — 1 пакетик в день, от 1 до 2 лет — 2 пакетика в день). p Пеногасители: эспумизан (с жидкостью после еды по 1 ч. л. 3 -5 раз в день). p Эубиотики: линекс (по 1 капсуле 1 -3 раза в сутки) и др. . Антибактериальные препараты при неинфекционных диареях не назначают!
Медикаментозная терапия p Ферментотерапия: микрокапсулированный препарат панкреатина — креон (по 1 капсуле 3 — 4 раза в сутки во время еды, содержимое капсулы смешивается с небольшим количеством пищи). p Энтеросорбенты: смекта (до 1 года жизни — 1 пакетик в день, от 1 до 2 лет — 2 пакетика в день). p Пеногасители: эспумизан (с жидкостью после еды по 1 ч. л. 3 -5 раз в день). p Эубиотики: линекс (по 1 капсуле 1 -3 раза в сутки) и др. . Антибактериальные препараты при неинфекционных диареях не назначают!  Хронические расстройства питания у детей раннего возраста p Дистрофии – патологические состояния вследствие недостаточного или избыточного поступления и/или усвоения питательных веществ. p Группировка дистрофий у детей первых двух лет жизни: Ø Гипотрофия — отставание массы в сравнении с ростом. Ø Гипостатура — равномерное отставание массы и роста. Ø Паратрофия — избыток массы по отношению к росту.
Хронические расстройства питания у детей раннего возраста p Дистрофии – патологические состояния вследствие недостаточного или избыточного поступления и/или усвоения питательных веществ. p Группировка дистрофий у детей первых двух лет жизни: Ø Гипотрофия — отставание массы в сравнении с ростом. Ø Гипостатура — равномерное отставание массы и роста. Ø Паратрофия — избыток массы по отношению к росту.  Экзогенные причины гипотрофий: p Голодание: количественный недокорм (при гипогалактии у матери, затруднениях при вскармливании (плоский сосок, «тугая» молочная железа у матери, «короткая уздечка» языка, частые срыгивания у ребенка и т. д. )), качественный недокорм (использование несоответствующей возрасту смеси; позднее введение прикормов и т. д. ). p Тяжёлая психосоциальная депривация (когда ребенок не получает достаточного внимания, ласки, психогенной стимуляции развития, умышленно жестокое обращение с ребёнком). p Инфекционные заболевания (хронические воспалительные заболевания, СПИД). p Токсические факторы (использование при искусственном вскармливании смесей с истекшим сроком хранения, гипервитаминозы А и Д, отравления, в том числе и лекарственные).
Экзогенные причины гипотрофий: p Голодание: количественный недокорм (при гипогалактии у матери, затруднениях при вскармливании (плоский сосок, «тугая» молочная железа у матери, «короткая уздечка» языка, частые срыгивания у ребенка и т. д. )), качественный недокорм (использование несоответствующей возрасту смеси; позднее введение прикормов и т. д. ). p Тяжёлая психосоциальная депривация (когда ребенок не получает достаточного внимания, ласки, психогенной стимуляции развития, умышленно жестокое обращение с ребёнком). p Инфекционные заболевания (хронические воспалительные заболевания, СПИД). p Токсические факторы (использование при искусственном вскармливании смесей с истекшим сроком хранения, гипервитаминозы А и Д, отравления, в том числе и лекарственные).  Эндогенные причины гипотрофий: p Нарушения обмена веществ (галактоземия, фруктоземия, лейциноз, болезни Ниманна-Пика, Тея-Сакса и др. ) p Иммунодефицитные состояния. p Анатомические нарушения ЖКТ (гастроэзофагальный рефлюкс, пилороспазм, долихосигма, болезнь Гиршпрунга и др. ). p Патология ЦНС (ППЦНС, родовая травма, ДЦП, нервно- мышечные заболевания). p Врождённая патология сердца и лёгких сопровождающаяся хронической СН или ДН (аномалии развития лёгких, врождённые пороки сердца). p Нарушения всасывания пищи: ферментопатии , муковисцидоз, количественная недостаточность клеток слизистой кишечника при алкогольном синдроме плода. p Эндокринные заболевания (гипертиреоз, гиперпаратиреоидизм, сахарный диабет, адреногенитальный синдром и др. ).
Эндогенные причины гипотрофий: p Нарушения обмена веществ (галактоземия, фруктоземия, лейциноз, болезни Ниманна-Пика, Тея-Сакса и др. ) p Иммунодефицитные состояния. p Анатомические нарушения ЖКТ (гастроэзофагальный рефлюкс, пилороспазм, долихосигма, болезнь Гиршпрунга и др. ). p Патология ЦНС (ППЦНС, родовая травма, ДЦП, нервно- мышечные заболевания). p Врождённая патология сердца и лёгких сопровождающаяся хронической СН или ДН (аномалии развития лёгких, врождённые пороки сердца). p Нарушения всасывания пищи: ферментопатии , муковисцидоз, количественная недостаточность клеток слизистой кишечника при алкогольном синдроме плода. p Эндокринные заболевания (гипертиреоз, гиперпаратиреоидизм, сахарный диабет, адреногенитальный синдром и др. ). 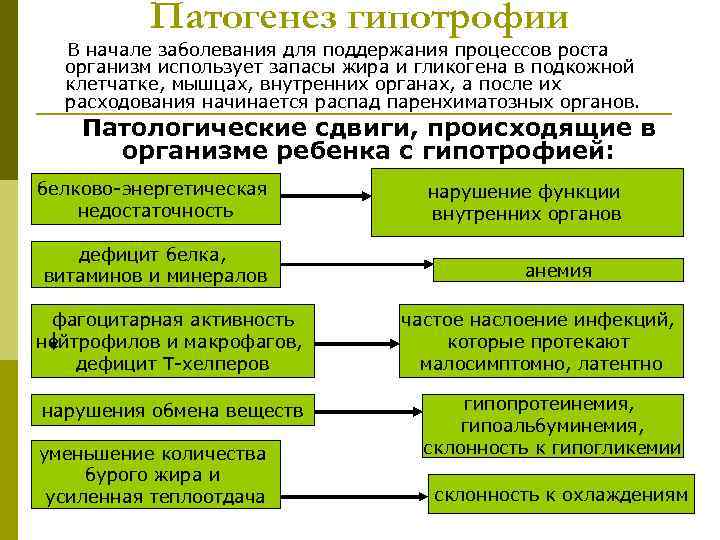 Патогенез гипотрофии В начале заболевания для поддержания процессов роста организм использует запасы жира и гликогена в подкожной клетчатке, мышцах, внутренних органах, а после их расходования начинается распад паренхиматозных органов. Патологические сдвиги, происходящие в организме ребенка с гипотрофией: белково-энергетическая нарушение функции недостаточность внутренних органов дефицит белка, витаминов и минералов анемия фагоцитарная активность частое наслоение инфекций, нейтрофилов и макрофагов, которые протекают дефицит Т-хелперов малосимптомно, латентно нарушения обмена веществ гипопротеинемия, гипоальбуминемия, уменьшение количества склонность к гипогликемии бурого жира и усиленная теплоотдача склонность к охлаждениям
Патогенез гипотрофии В начале заболевания для поддержания процессов роста организм использует запасы жира и гликогена в подкожной клетчатке, мышцах, внутренних органах, а после их расходования начинается распад паренхиматозных органов. Патологические сдвиги, происходящие в организме ребенка с гипотрофией: белково-энергетическая нарушение функции недостаточность внутренних органов дефицит белка, витаминов и минералов анемия фагоцитарная активность частое наслоение инфекций, нейтрофилов и макрофагов, которые протекают дефицит Т-хелперов малосимптомно, латентно нарушения обмена веществ гипопротеинемия, гипоальбуминемия, уменьшение количества склонность к гипогликемии бурого жира и усиленная теплоотдача склонность к охлаждениям  Классификация гипотрофий по степень тяжести p 1 ст. (легкая) p 2 ст. (средней тяжести) p 3 ст. (тяжелая – атрепсия)
Классификация гипотрофий по степень тяжести p 1 ст. (легкая) p 2 ст. (средней тяжести) p 3 ст. (тяжелая – атрепсия)  Гипотрофия 1 степени Общее состояние ребёнка страдает мало, психомоторное развитие соответствует возрасту. Иммунологическая реактивность и толерантность к пище, как правило, не изменена. Симптомы: p лёгкая бледность кожных покровов, снижение их эластичности, p истончение подкожно-жировой клетчатки в области туловища, p снижение массы тела на 11 -20% от должной (рост при этом не отстает от нормы), массо-ростовой коэффициент – 56 -60 (в норме более 60), p умеренное двигательное беспокойство, раздражительность, p урежение дефекаций, p гипоальбуминемия.
Гипотрофия 1 степени Общее состояние ребёнка страдает мало, психомоторное развитие соответствует возрасту. Иммунологическая реактивность и толерантность к пище, как правило, не изменена. Симптомы: p лёгкая бледность кожных покровов, снижение их эластичности, p истончение подкожно-жировой клетчатки в области туловища, p снижение массы тела на 11 -20% от должной (рост при этом не отстает от нормы), массо-ростовой коэффициент – 56 -60 (в норме более 60), p умеренное двигательное беспокойство, раздражительность, p урежение дефекаций, p гипоальбуминемия.  Гипотрофия 2 степени Симптомы: p выраженная бледность, сухость и шелушение кожи p истончение подкожно-жировой клетчатки на животе, туловище и конечностях, p снижение тургора тканей и тонуса мышц, p блеклость, ломкость волос, p отставание в массе на 20 -30% (по отношению к длине), в росте на 2 -4 см, p плохой аппетит, снижение толерантности к пище, периодические рвоты, p отставание в психомоторном развитии, p нарушение сна, p нарушение терморегуляции, p неустойчивый стул: запор-понос, развитие дисбактериоза разной степени выраженности, p изменения в копрограмме (крахмал, нейтральный жир, слизь, мышечные волокна, лимфоциты), p появление у мочи запаха аммиака, p резкое снижение иммунологической толерантности, малосимптомное и атипичное течение соматической патологии.
Гипотрофия 2 степени Симптомы: p выраженная бледность, сухость и шелушение кожи p истончение подкожно-жировой клетчатки на животе, туловище и конечностях, p снижение тургора тканей и тонуса мышц, p блеклость, ломкость волос, p отставание в массе на 20 -30% (по отношению к длине), в росте на 2 -4 см, p плохой аппетит, снижение толерантности к пище, периодические рвоты, p отставание в психомоторном развитии, p нарушение сна, p нарушение терморегуляции, p неустойчивый стул: запор-понос, развитие дисбактериоза разной степени выраженности, p изменения в копрограмме (крахмал, нейтральный жир, слизь, мышечные волокна, лимфоциты), p появление у мочи запаха аммиака, p резкое снижение иммунологической толерантности, малосимптомное и атипичное течение соматической патологии.  Гипотрофия 3 степени p Симптомы: p выраженная бледность кожи с серым оттенком, резкое снижение эластичности p полное отсутствие подкожно-жирового слоя, p атрофия мышц, p отставание в массе тела свыше 30%, отставание в росте – более 4 см, p общая вялость, снижение интереса к окружающему, отсутствие активных движений, p страдальческое выражение на лице, а в терминальный период — безразличие, p резкое нарушение терморегуляции, быстрое охлаждение, p задержка психомоторного развития, p дыхание поверхностное, иногда могут отмечаться апноэ, p тоны сердца ослабленные, глухие, может наблюдаться тенденция к брадикардии, артериальной гипотонии, p живот увеличен в объёме вследствие метеоризма, передняя брюшная стенка истончена, контурируются петли кишок, запоры чередуются с мыльно-известковыми опорожнениями, p анорексия, ослабление жажды, нарушение толерантности к пище
Гипотрофия 3 степени p Симптомы: p выраженная бледность кожи с серым оттенком, резкое снижение эластичности p полное отсутствие подкожно-жирового слоя, p атрофия мышц, p отставание в массе тела свыше 30%, отставание в росте – более 4 см, p общая вялость, снижение интереса к окружающему, отсутствие активных движений, p страдальческое выражение на лице, а в терминальный период — безразличие, p резкое нарушение терморегуляции, быстрое охлаждение, p задержка психомоторного развития, p дыхание поверхностное, иногда могут отмечаться апноэ, p тоны сердца ослабленные, глухие, может наблюдаться тенденция к брадикардии, артериальной гипотонии, p живот увеличен в объёме вследствие метеоризма, передняя брюшная стенка истончена, контурируются петли кишок, запоры чередуются с мыльно-известковыми опорожнениями, p анорексия, ослабление жажды, нарушение толерантности к пище  Принципы лечения гипотрофии
Принципы лечения гипотрофии  Принципы диетотерапии p Омоложение диеты p Увеличение частоты кормлений p Принцип трехфазного питания: Ø адаптационный период (определяется толерантность ребенка к пищевой нагрузке и проводится коррекция водно-минерального обмена), Ø репарационный период (осуществляется коррекция белков, жиров и углеводов), Ø период усиленного питания (проводится повышенная энергетическая нагрузка). p Адекватный систематический контроль питания (ведение дневника с отметкой количества съеденной в каждое кормление пищи), стула, диуреза, количества выпитой и даваемой парентерально жидкости, солей и др. ; регулярный (раз в 5 -7 дней) расчет пищевой нагрузки по белкам, жирам, углеводам; дважды в неделю – копрограмма.
Принципы диетотерапии p Омоложение диеты p Увеличение частоты кормлений p Принцип трехфазного питания: Ø адаптационный период (определяется толерантность ребенка к пищевой нагрузке и проводится коррекция водно-минерального обмена), Ø репарационный период (осуществляется коррекция белков, жиров и углеводов), Ø период усиленного питания (проводится повышенная энергетическая нагрузка). p Адекватный систематический контроль питания (ведение дневника с отметкой количества съеденной в каждое кормление пищи), стула, диуреза, количества выпитой и даваемой парентерально жидкости, солей и др. ; регулярный (раз в 5 -7 дней) расчет пищевой нагрузки по белкам, жирам, углеводам; дважды в неделю – копрограмма.  Адаптационный период (период выяснения толерантности к пище) Длится: n при гипотрофии 1 степени – 1 -2 дня, n при гипотрофии 2 степени – 3 -7 дней, n при гипотрофии 3 степени – 10 -14 дней. На начальных этапах лечения применяется лишь легкоусвояемая пища: n ребенка кормят женским молоком, n при его отсутствии – адаптированными молочными смесями, лучше — гипоаллергенными (НАН ГА, ХИПП ГА) или кисломолочными (Галлия Лактофидус, НАН кисломолочный). Увеличивают частоту кормлений: n при гипотрофии 1 степени – 7, n при гипотрофии 2 степени – 8, n при гипотрофии 3 степени – 10 -12.
Адаптационный период (период выяснения толерантности к пище) Длится: n при гипотрофии 1 степени – 1 -2 дня, n при гипотрофии 2 степени – 3 -7 дней, n при гипотрофии 3 степени – 10 -14 дней. На начальных этапах лечения применяется лишь легкоусвояемая пища: n ребенка кормят женским молоком, n при его отсутствии – адаптированными молочными смесями, лучше — гипоаллергенными (НАН ГА, ХИПП ГА) или кисломолочными (Галлия Лактофидус, НАН кисломолочный). Увеличивают частоту кормлений: n при гипотрофии 1 степени – 7, n при гипотрофии 2 степени – 8, n при гипотрофии 3 степени – 10 -12.  Адаптационный период (продолжение) В первый день выяснения толерантности к пище назначают уменьшенный объем питания: n при гипотрофии 1 степени – до 2/3 от необходимого суточного объема, n при гипотрофии 2 степени – ½-2/3 от необходимого суточного объема, n при гипотрофии 3 степени – ½ от необходимого суточного объема. Недостающий объем восполняют жидкостью в виде глюкозо- солевых растворов: n оралит, n регидрон, n цитроглюкосолан. При улучшении аппетита, количество основной молочной смеси постепенно увеличивают (примерно по 10 -20 мл на кормление ежедневно), доводя его в конце адаптационного периода до должного, но не более 1 литра. Адаптационный период заканчивается при достижении необходимого суточного объема пищи и расчете белков, жиров и углеводов на фактическую массу тела ребенка.
Адаптационный период (продолжение) В первый день выяснения толерантности к пище назначают уменьшенный объем питания: n при гипотрофии 1 степени – до 2/3 от необходимого суточного объема, n при гипотрофии 2 степени – ½-2/3 от необходимого суточного объема, n при гипотрофии 3 степени – ½ от необходимого суточного объема. Недостающий объем восполняют жидкостью в виде глюкозо- солевых растворов: n оралит, n регидрон, n цитроглюкосолан. При улучшении аппетита, количество основной молочной смеси постепенно увеличивают (примерно по 10 -20 мл на кормление ежедневно), доводя его в конце адаптационного периода до должного, но не более 1 литра. Адаптационный период заканчивается при достижении необходимого суточного объема пищи и расчете белков, жиров и углеводов на фактическую массу тела ребенка.  Репарационный период (промежуточный или переходный). p Постепенно увеличивают пищевую нагрузку белками, углеводами и, в последнюю очередь, жирами. Для этого к грудному молоку или заменяющей его смеси постепенно добавляют соответствующие лечебные смеси (до 1/3 общего объема). Начинают вводить прикормы, если это положено по возрасту. p В репарационный период белки и углеводы рассчитываю на приблизительно долженствующую массу, которая определяется по следующей схеме: n на 1 -й неделе приблизительно долженствующая масса равна фактической массе ребенка + 5% от нее; n на 2 -й неделе – к фактической массе прибавляется 10%; n на 3 -й неделе – 15% и на 4 -й неделе – 20%. p В течение всего репарационного периода жиры рассчитываются на фактическую массу ребенка.
Репарационный период (промежуточный или переходный). p Постепенно увеличивают пищевую нагрузку белками, углеводами и, в последнюю очередь, жирами. Для этого к грудному молоку или заменяющей его смеси постепенно добавляют соответствующие лечебные смеси (до 1/3 общего объема). Начинают вводить прикормы, если это положено по возрасту. p В репарационный период белки и углеводы рассчитываю на приблизительно долженствующую массу, которая определяется по следующей схеме: n на 1 -й неделе приблизительно долженствующая масса равна фактической массе ребенка + 5% от нее; n на 2 -й неделе – к фактической массе прибавляется 10%; n на 3 -й неделе – 15% и на 4 -й неделе – 20%. p В течение всего репарационного периода жиры рассчитываются на фактическую массу ребенка. 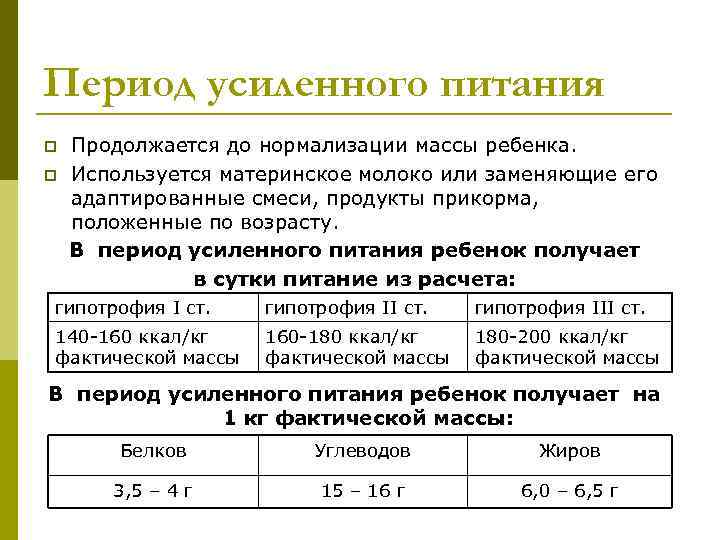 Период усиленного питания p Продолжается до нормализации массы ребенка. p Используется материнское молоко или заменяющие его адаптированные смеси, продукты прикорма, положенные по возрасту. В период усиленного питания ребенок получает в сутки питание из расчета: гипотрофия I ст. гипотрофия III ст. 140 -160 ккал/кг 160 -180 ккал/кг 180 -200 ккал/кг фактической массы В период усиленного питания ребенок получает на 1 кг фактической массы: Белков Углеводов Жиров 3, 5 – 4 г 15 – 16 г 6, 0 – 6, 5 г
Период усиленного питания p Продолжается до нормализации массы ребенка. p Используется материнское молоко или заменяющие его адаптированные смеси, продукты прикорма, положенные по возрасту. В период усиленного питания ребенок получает в сутки питание из расчета: гипотрофия I ст. гипотрофия III ст. 140 -160 ккал/кг 160 -180 ккал/кг 180 -200 ккал/кг фактической массы В период усиленного питания ребенок получает на 1 кг фактической массы: Белков Углеводов Жиров 3, 5 – 4 г 15 – 16 г 6, 0 – 6, 5 г  Организация режима при гипотрофии p Температуру воздуха в палатах необходимо поддерживать постоянной (+24…+25°С). p Палаты следует проветривать 5 -6 раз в сутки. Должны быть организованы прогулки на свежем воздухе. p Должны проводиться регулярные гигиенические процедуры: подмывание, купание. Температура воды в ванне во время купания должна быть 38°С. p Все дети должны достаточно спать. p В период бодрствования рекомендуется чаще брать ребенка на руки, менять положение его тела в кроватке, выкладывать в манеж. p Важным моментом является поднятие эмоционального статуса ребенка. Положительное влияние оказывают ласковая речь, разнообразные игрушки, красивая музыка. p Необходимо ограждать ребенка от громких слов, стуков, яркого света – все это может усилить тормозные процессы в ЦНС. p Обязательными в лечении детей с гипотрофией являются массаж и гимнастика.
Организация режима при гипотрофии p Температуру воздуха в палатах необходимо поддерживать постоянной (+24…+25°С). p Палаты следует проветривать 5 -6 раз в сутки. Должны быть организованы прогулки на свежем воздухе. p Должны проводиться регулярные гигиенические процедуры: подмывание, купание. Температура воды в ванне во время купания должна быть 38°С. p Все дети должны достаточно спать. p В период бодрствования рекомендуется чаще брать ребенка на руки, менять положение его тела в кроватке, выкладывать в манеж. p Важным моментом является поднятие эмоционального статуса ребенка. Положительное влияние оказывают ласковая речь, разнообразные игрушки, красивая музыка. p Необходимо ограждать ребенка от громких слов, стуков, яркого света – все это может усилить тормозные процессы в ЦНС. p Обязательными в лечении детей с гипотрофией являются массаж и гимнастика.  Основные направления медикаментозной терапии при гипотрофии p Ферментотерапия проводится в основном препаратами поджелудочной железы: креоном, панзинормом, панцитратом, панкреатином. p Биопрепараты назначаются при дисбактериозе кишечника: бифидумбактерин, бификол, бифилиз, бифиформ, лактобактерин. p Витаминотерапия В первые дни применяют витамины С, В 1, В 6. , во 2 -й и 3 -й периоды диетотерапии проводят чередующиеся курсы витаминов А, PP, B 15, B 5, E, фолиевой кислоты, В 12. p Стимулирующая и иммунотерапия. Можно использовать 20% раствор карнитина хлорида (по 1 капле/кг массы тела 3 раза в день внутрь) в течение месяца. В период разгара гипотрофии, сопровождающейся наслоением инфекции, вводятся внутривенно иммуноглобулины.
Основные направления медикаментозной терапии при гипотрофии p Ферментотерапия проводится в основном препаратами поджелудочной железы: креоном, панзинормом, панцитратом, панкреатином. p Биопрепараты назначаются при дисбактериозе кишечника: бифидумбактерин, бификол, бифилиз, бифиформ, лактобактерин. p Витаминотерапия В первые дни применяют витамины С, В 1, В 6. , во 2 -й и 3 -й периоды диетотерапии проводят чередующиеся курсы витаминов А, PP, B 15, B 5, E, фолиевой кислоты, В 12. p Стимулирующая и иммунотерапия. Можно использовать 20% раствор карнитина хлорида (по 1 капле/кг массы тела 3 раза в день внутрь) в течение месяца. В период разгара гипотрофии, сопровождающейся наслоением инфекции, вводятся внутривенно иммуноглобулины.  Паратрофия – это хроническое расстройство питания, сопровождающееся нарушением обменных функций организма и характеризующееся избыточной массой тела и повышенной гидролабильностью тканей. Основными причинами развития паратрофии являются: p злоупотребление высококалорийными продуктами (злоупотребление кашей и хлебобулочными изделиями, использование приготовлении адаптированных смесей большего количества сухого порошка, чем положено), p высокобелковое питание (большое количество цельного коровьего молока, творога), p эндокринные и нейроэндокринные расстройства.
Паратрофия – это хроническое расстройство питания, сопровождающееся нарушением обменных функций организма и характеризующееся избыточной массой тела и повышенной гидролабильностью тканей. Основными причинами развития паратрофии являются: p злоупотребление высококалорийными продуктами (злоупотребление кашей и хлебобулочными изделиями, использование приготовлении адаптированных смесей большего количества сухого порошка, чем положено), p высокобелковое питание (большое количество цельного коровьего молока, творога), p эндокринные и нейроэндокринные расстройства.  Клиника паратрофии Наиболее характерными симптомами паратрофии являются: p равномерная избыточная масса тела, p повышенное отложение подкожного жира, p бледность кожных покровов, p признаки мышечной гипотонии, отставание в моторном развитии (дети малоподвижны), p приглушенность тонов сердца, систолический шум, p бродильная диспепсия, вздутие живота, умеренно выраженный токсикоз за счет всасывания органических кислот.
Клиника паратрофии Наиболее характерными симптомами паратрофии являются: p равномерная избыточная масса тела, p повышенное отложение подкожного жира, p бледность кожных покровов, p признаки мышечной гипотонии, отставание в моторном развитии (дети малоподвижны), p приглушенность тонов сердца, систолический шум, p бродильная диспепсия, вздутие живота, умеренно выраженный токсикоз за счет всасывания органических кислот.  Степени паратрофии: p 1 ст. – избыточная масса тела 10 -20%, p 2 ст. – избыточная масса тела 25 -35%, p 3 ст. – избыточная масса тела 40 -50%.
Степени паратрофии: p 1 ст. – избыточная масса тела 10 -20%, p 2 ст. – избыточная масса тела 25 -35%, p 3 ст. – избыточная масса тела 40 -50%.  Лечение паратрофии включает: p Оптимальная диетотерапия, p Организация режима, ухода, массажа, ЛФК, p Медикаментозная терапия.
Лечение паратрофии включает: p Оптимальная диетотерапия, p Организация режима, ухода, массажа, ЛФК, p Медикаментозная терапия.  Проведение этапного диетического лечения включает: p I этап (разгрузки) длится 7 -10 дней, предусматривает отмену высококалорийных продуктов, следует использовать овощи и несладкие сорта фруктов. Общий объем пищи соответствует возрастным нормам. Лучшим продуктом является женское молоко, при его отсутствии – кисломолочные смеси (НАН кисломолочный, Лактофидус). p II этап (переходный) длится 3 -4 недели. Ребенку первых 4 месяцев жизни вводят соответствующие возрасту прикормы, начиная с овощного пюре. p III этап (минимально-оптимальной диеты) – ребенок получает все низкокалорийные виды прикорма, соответствующие возрасту. Расчет необходимого количества белка проводится на фактическую массу, жиров, углеводов и калорий – на долженствующую. При искусственном вскармливании — смесь с низким (по отношению к другим смесям) содержанием белка (НАН 1 — 1, 2 г на 100 мл)
Проведение этапного диетического лечения включает: p I этап (разгрузки) длится 7 -10 дней, предусматривает отмену высококалорийных продуктов, следует использовать овощи и несладкие сорта фруктов. Общий объем пищи соответствует возрастным нормам. Лучшим продуктом является женское молоко, при его отсутствии – кисломолочные смеси (НАН кисломолочный, Лактофидус). p II этап (переходный) длится 3 -4 недели. Ребенку первых 4 месяцев жизни вводят соответствующие возрасту прикормы, начиная с овощного пюре. p III этап (минимально-оптимальной диеты) – ребенок получает все низкокалорийные виды прикорма, соответствующие возрасту. Расчет необходимого количества белка проводится на фактическую массу, жиров, углеводов и калорий – на долженствующую. При искусственном вскармливании — смесь с низким (по отношению к другим смесям) содержанием белка (НАН 1 — 1, 2 г на 100 мл)  Гипостатура – это хроническое расстройство питания, характеризующееся более или менее равномерным отставанием в росте и массе тела при несколько сниженном состоянии упитанности и тургора тканей. Гипостатура характерна для детей p с врожденными пороками сердца, p с пороками развития ЦНС, p с энцефалопатиями и эндокринной патологией. После лечения основного заболевания физическое развитие ребенка нормализуется.
Гипостатура – это хроническое расстройство питания, характеризующееся более или менее равномерным отставанием в росте и массе тела при несколько сниженном состоянии упитанности и тургора тканей. Гипостатура характерна для детей p с врожденными пороками сердца, p с пороками развития ЦНС, p с энцефалопатиями и эндокринной патологией. После лечения основного заболевания физическое развитие ребенка нормализуется.  Литература p Вскармливание грудных детей с пищевой непереносимостью /Е. И. Капранова. – Москва. 2003. – 33 с. p Демин В. Ф. , Ключникова С. О. , Цветкова Л. Н. , Мухина Ю. Г. Лекции по педиатрии. Том 3. Гастроэнтерология. М. , 2003, с. 112 – 135, 152 – 162. p Практическое руководство по детским болезням под общей ред. В. Ф. Коколиной и А. Г. Румянцева, «Неотложная педиатрия» под ред. Б. М. Блохина, Москва 2005 г. p Рациональная фармакотерапия заболеваний органов пищеварения: Рук. Для практикующих врачей / В. Т. Ивашкин, Т. Л. Лапина и др. ; Под общ. Ред. В. Т. Ивашкина. – М. : Литтерра, 2003. – С. 465 -473. p Руководство по детскому питанию / Под ред. В. А. Тутельяна, И. Я. Коня. – М. : Медицинское информационное агентство, 2004. – 662 с. : табл.
Литература p Вскармливание грудных детей с пищевой непереносимостью /Е. И. Капранова. – Москва. 2003. – 33 с. p Демин В. Ф. , Ключникова С. О. , Цветкова Л. Н. , Мухина Ю. Г. Лекции по педиатрии. Том 3. Гастроэнтерология. М. , 2003, с. 112 – 135, 152 – 162. p Практическое руководство по детским болезням под общей ред. В. Ф. Коколиной и А. Г. Румянцева, «Неотложная педиатрия» под ред. Б. М. Блохина, Москва 2005 г. p Рациональная фармакотерапия заболеваний органов пищеварения: Рук. Для практикующих врачей / В. Т. Ивашкин, Т. Л. Лапина и др. ; Под общ. Ред. В. Т. Ивашкина. – М. : Литтерра, 2003. – С. 465 -473. p Руководство по детскому питанию / Под ред. В. А. Тутельяна, И. Я. Коня. – М. : Медицинское информационное агентство, 2004. – 662 с. : табл. 

